近年来,建筑装璜装饰材料进入家庭,调查发现经过装修的居室中由装璜装饰材料缓慢释放出来的化学污染物浓度过高,影响健康。这些污染物中最常见的是
| A.CO | B.SO2 | C.甲醛、甲苯等有机物蒸汽 | D.臭氧 |
为确定某溶液的离子组成,进行如下实验:
①测定溶液的pH,溶液显强碱性。
②取少量溶液加入稀盐酸至溶液呈酸性,产生无刺激性、能使澄清石灰水变浑浊的气体。
③在上述溶液中再滴加Ba(NO3)2溶液,产生白色沉淀。
④取上层清液继续滴加Ba(NO3)2溶液至无沉淀时,再滴加AgNO3溶液,产生白色沉淀。
根据实验以下推测正确的是:
| A.一定存在SO32-离子 | B.一定存在CO32-离子 |
| C.一定存在Cl-离子 | D.可能存在HCO3-离子 |
设阿伏加德常数为NA,则下列说法正确的是:
| A.常温常压下,11.2L甲烷中含有的氢原子数为2NA |
| B.标准状况下,0.3mol二氧化硫中含有氧原子数为0.3NA |
| C.常温下,2.7g铝与足量的盐酸反应,失去的电子数为0.3NA |
| D.常温下,1L 0.1 mol?L-1AlCl3溶液中含Al3+ 数为0.1NA |
下列推断合理的是()
| A.在常温下,Na2SiO3+H2O+CO2 = Na2CO3+H2SiO3↓,说明H2CO3酸性强于H2SiO3; 在高温下,Na2CO3+SiO2= Na2SiO3+CO  2↑,说明H2SiO3酸性强于H2CO3 2↑,说明H2SiO3酸性强于H2CO3 |
| B.c(NH4+)相等的(NH4)2SO4、(NH4)2CO3、(NH4)2Fe(SO4)2溶液,则 c[(NH4)2SO4]>c[(NH4)2CO3] >c[(NH4)2Fe(SO4)2] |
| C.向1L0.3mol/L的NaOH溶液中缓慢通入CO2气体至溶液增重8.8g时,则溶液中 2c(Na+)=3[c(HCO3-)+c(CO32-)+c(H2CO3)] |
| D.在海带中提取碘的实验中既可以用四氯化碳作萃取剂也可以用酒精作萃取剂 |
对某酸性溶液(可能含有Br-,SO42-,H2SO3,NH4+)分别进行如下实验:
①加热时放出的气体可以使品红溶液褪色
②加碱调至碱性后,加热时放出的气体可以使润湿的红色石蕊试纸变蓝;
③加入氯水和四氯化碳时,下层显橙色,再加入BaCl2溶液时,产生的白色沉淀不溶于稀硝酸
对于下列物质不能确认其在溶液中是否存在的是
A Br- B SO42- C H2SO3 D NH4+
关于下列各装置图的叙述中,不正确的是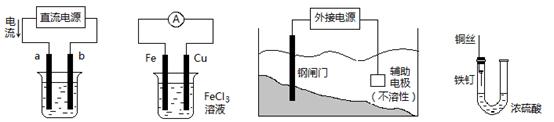
①②③④
| A.用装置①精炼铜,则a极为粗铜,电解质溶液为CuSO4溶液 |
| B.装置②的总反应是:Cu+2Fe3+=Cu2++2Fe2+ |
| C.装置③中钢闸门应与外接电源的负极相连 |
| D.装置④中的铁钉几乎没被腐蚀 |