下列离子方程式不正确的是
A.硫酸氢钠溶液中滴加Ba(OH)2溶液至呈中性 |
| B.FeCl3溶液中加入足量的Na2S溶液: 2Fe3++3S2-==2FeS↓+S↓ |
C.0.05 mol/LCa(H2PO4)2溶液与0.15 mol/L NaOH以等体积混合: +9H2O +9H2O |
| D.实验室用FeS与稀盐酸制取H2S气体: |
S2-+2H+====H2S↑
下列说法正确的是
| A.漂白液中添加醋酸可提高漂白速率 |
| B.石油裂化是为了除去石油中的杂质 |
| C.淀粉溶液可鉴别加碘盐的真伪 |
| D.蛋白质、淀粉、纤维素都能在人体内水解并提供能量 |
在密闭容器中通入NO和CO各2mol发生反应: 2NO(g)+ 2CO(g)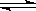 2CO2(g)+ N2(g)
2CO2(g)+ N2(g)
容器内CO2随温度(T)、压强(P)和时间(t)的变化曲线如下图所示。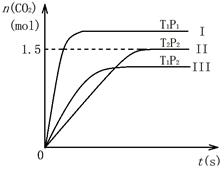
以下说法合理的是
| A.温度T2>T1 |
| B.压强P2>P1 |
| C.II曲线表示NO平衡转化率为25% |
| D.该反应的焓变△H<0 |
一种使用阴离子交换膜(只也许阴离子通过)的铜锌电池结构结构如下图: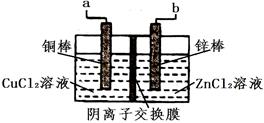
以下选项两栏内容正确且相关联的是
| 选项 |
操作与现象 |
解释与推论 |
| A |
电池放电时化学能转化为电能 |
Zn(s)+ Cu2+(aq)= Zn2+ + Cu(s)△H>0 |
| B |
该电池充电时铜棒变细 |
两电极区溶液颜色都变深 |
| C |
该电池放电时铜棒是电池正极 |
Cl-通过交换膜从左(铜棒区)向右(锌棒区)移动 |
| D |
该电池充电时a接电源正极 |
电极反应Cu2++2e- = Cu |
0.1 mol•L-1 AlCl3溶液,温度从20℃升高到50℃,浓度增幅最大的离子是
| A.Cl- | B.Al3+ | C.H+ | D.OH- |
下列离子方程式正确的是
| A.向Ba(OH)2溶液中滴入硫酸溶液:Ba2++SO42-= BaSO4↓ |
| B.向Na2CO3溶液中通入过量CO2气体:CO32-+CO2+H2O=2HCO3— |
| C.BaCO3溶于醋酸溶液:BaCO3+2H+=Ba2++H2O+CO2↑ |
| D.金属铝溶于氢氧化钠溶液: Al + 2OH-= AlO2- + H2↑ |