含有2~5个碳原子的直链烷烃沸点和燃烧热的数据见下表:
| 烷烃名称 |
乙烷 |
丙烷 |
丁烷 |
戊烷 |
| 沸点/℃ |
-88.6 |
-42.1 |
-0.5 |
36.1 |
| 燃烧热/kJ· moL-1 |
1 560.7 |
2 219.2 |
2 877.6 |
3 535.6 |
根据表中数据,下列判断错误的是( )
| A.正庚烷在常温常压下肯定不是气体 |
| B.随碳原子数增多,烷烃燃烧热增大 |
| C.随碳原子数增加,烷烃沸点逐渐升高 |
| D.随碳原子数增加,烷烃沸点和燃烧热都成比例增大 |
如图所示,把下列物质分别加入装有水的锥形瓶里,立即塞紧带有U形管的塞子,已知U形管内预先装有少量水(为方便观察,预先将水染成红色),结果U形管左边液面升高,则加入的物质可能是( ) 
| A.NaOH固体 | B.浓硫酸 | C.NH4NO3晶体 | D.Na2O2固体 |
碱性电池具有容量大、放电电流大的特点,因而得到广泛应用。锌—锰碱性电池以氢氧化钾溶液为电解液,电池总反应式为: Zn(s)+2MnO2(s)+H2O(l)==Zn(OH)2(s)+Mn2O3(s) ,下列说法错误的是( )
| A.电池工作时,锌失去电子 |
| B.电池正极的电极反应式为:2MnO2(s)+H2O(1)+2e—=Mn2O3(s)+2OH—(aq) |
| C.电池工作时,电子由正极通过外电路流向负极 |
| D.外电路中每通过0.2mol电子,锌的质量理论上减小6.5g |
某元素的一种同位素X原子的质量数为A,含N个中子,它与H原子组成HmX分子,在ag HmX分子中含质子的物质的量是 ( )
A.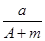 (A-N+m) mol (A-N+m) mol |
B. (A-N) mol (A-N) mol |
C.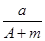 ( A-N) mol ( A-N) mol |
D. (A-N+m) mol (A-N+m) mol |
目前,人类已经发现的非金属元素除稀有气体元素外共有16种,下列对这16种非金属元素的判断不正确的是()
①都是主族元素,原子的最外层电子数都大于3②单质在反应中都只能作氧化剂
③对应的含氧酸都是强酸④氢化物常温下都是气态,所以又叫气态氢化物
⑤气态氧化物与水反应都不会再生成气体
| A.全部 | B.只有①② | C.只有①②③④ | D.只有①②④⑤ |
根据表中信息,判断以下叙述正确的是( )
部分短周期元素的原子半径及主要化合价
| 元素代号 |
L |
M |
Q |
R |
T |
| 原子半径/nm |
0.160 |
0.143 |
0.112 |
0.104 |
0.066 |
| 主要化合价 |
+2 |
+3 |
+2 |
+6、-2 |
-2 |
A.氢化物的稳定性为H2T<H2R B.单质与稀盐酸反应的剧烈程度为L<Q
C.M与T形成的化合物具有两性 D.L2+与R2-的核外电子数相等