按如图所示的装置进行实验:A极是铜锌合金,B极是纯铜,电解质溶液中含有足量的铜离子,通电一段时间后,若A极恰好全部溶解,此时B极质量增加7.68g,溶液质量增加0.03 g,则A合金中Cu、Zn的物质的量之比为( )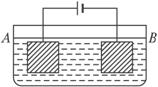
| A.4∶1 | B.3∶1 | C.2∶1 | D.1∶1 |
25℃时,在含有Pb2+、Sn2+的某溶液中,加入过量金属锡(Sn),发生反应:Sn(s)+Pb2+(aq) Sn2+(aq)+Pb(s),体系中c(Pb2+)和c(Sn2+)变化关系如右图所示。下列判断正确的是()
Sn2+(aq)+Pb(s),体系中c(Pb2+)和c(Sn2+)变化关系如右图所示。下列判断正确的是()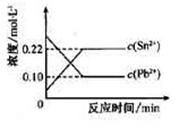
| A.往平衡体系中加入金属铅后,c(Pb2+)增大 |
| B.往平衡体系中加入少量Sn(NO3)2固体后,c(Pb2+)变小 |
| C.升高温度,平衡体系中c(Pb2+)增大,说明该反应△H>0 |
| D.25℃时,该反应的平衡常数K=2.2 |
下列图像分别表示有关反应的反应过程与能量变化的关系( )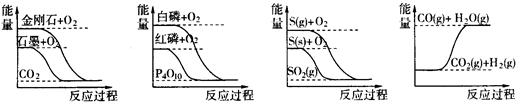
据此判断下列说法中正确的是( )
| A.石墨转变为金刚石是吸热反应 |
| B.S(g) + O2(g) ="==" SO2(g);△H1,S(s)+O2(g)===SO2(g);△H2,则△H1>△H2 |
| C.白磷比红磷稳定 |
| D.CO(g)+H2O(g)===CO2(g)+H2(g);△H1>0 |
已知汽车尾气无害化处理反应为( )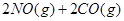

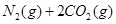 下列说法不正确的是
下列说法不正确的是
A.升高温度可使该反应的逆反应速率降低 |
B.使用高效催化剂可有效提高正反应速率 |
C.反应达到平衡后,N0的反应速率保持恒定 |
D.单位时间内消耗CO和CO2的物质的量相等时,反应达到平衡 |
一定温度下,某反应达到平衡,平衡常数K=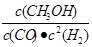 。恒容时,温度升高,H2浓度增大。下列说法正确的是()
。恒容时,温度升高,H2浓度增大。下列说法正确的是()
A.该反应的化学方程式为CH3OH CO+2H2 CO+2H2 |
B.使用催化剂,H2浓度一定减小 |
| C.升高温度,逆反应速率减小 | D.该反应的焓变(ΔH)为负值 |
某探究小组利用丙酮的溴代反应:( )
)
来研究反应物浓度与反应速率的关系。反应速率 通过测定溴的颜色消失所需的时间来确定。在一定温度下,获得如下实验数据( )
通过测定溴的颜色消失所需的时间来确定。在一定温度下,获得如下实验数据( )

 分析实验数据所得出的结论不正确的是
分析实验数据所得出的结论不正确的是
A.增大 增大 增大 |
B.实验②和③的 相等 相等 |
C.增大  增大 增大 |
D.增大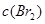 , , 增大 增大 |