下列有关稀有气体的描述不正确的是
①原子的最外层电子数都有8个 ②其原子与下周期第ⅠA族、ⅡA族的阳离子具有相同的电子层结构③有些稀有气体能跟某些物质反应 ④原子半径比同周期的元素的原子大
| A.只有① |
| B.①和③ |
| C.①和② |
| D.②和④ |
下列各组元素性质的递变情况错误的是 ( )
| A.Li、Be、B原子最外层电子数依次增多 | B.P、S、C1元素最高正价依次升高 |
| C.N、O、F原子半径依次增大 | D.Na、K、Rb的电子层数依次增多 |
氯化硼的熔点为-107℃,沸点为12.5℃,在其分子中键与键之间的夹角为120°,它能水解,有关叙述正确的是
A. 氯化硼液态时能导电而固态时不导电 氯化硼液态时能导电而固态时不导电 |
| B.氯化硼中心原子采用sp杂化 |
| C.氯化硼分子呈正三角形,属非极性分子 |
| D.其分子空间结构类似CH2O |
下列电子排布式中,原子处于激发状态的是
A.1s22s 22p5 22p5 |
B.1s22s22p43s2 |
| C.1s22s22p63s23p63d44s2 | D.1s22s22p63s23p63d34s2 |
下列有机物分子中带“*”碳原子就是手性碳原子。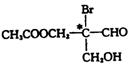
该有机物分别发生下列反应,生成的有机物分子中含有手性碳原子的是
| A.与乙酸发生酯化反应 | B.与NaOH水溶液反应 |
| C.与银氨溶液作用只发生银镜反应 | D.催化剂作用下与H2反应 |
已知次氯酸分子的结构式为H—O—Cl,下列有关说法正确的是
| A.次氯酸为非极性共价化合物 | B.O原子与H、Cl都形成σ键 |
| C.该分子为直线型分子 | D.该分子的电子式是H︰O︰Cl |