当反应L(s)+aG(g)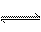 bR(g)达到平衡后,温度和压强对该反应的影响如下图所示,图中压强p1> p2,x轴表示温度,y轴表示平衡混合气中G的体积分数。据此可判断( )
bR(g)达到平衡后,温度和压强对该反应的影响如下图所示,图中压强p1> p2,x轴表示温度,y轴表示平衡混合气中G的体积分数。据此可判断( ) 
| A.上述反应是放热反应 | B.上述反应是吸热反应 |
| C.a>b | D.d<b |
研究表明:多种海产品体内含有+5价的砷(As)元素,对人体无毒,而砒霜的成分是As2O3,有剧毒;青菜中含有维生素C.专家忠告:不要同时大量食用海鲜和青菜,否则容易中毒。下面有关解释不正确的是()
A.As2O3中As元素为+3价
B.致人中毒过程中砷元素发生氧化反应
C.维生素C能将+5价砷还原成As2O3
D.维生素C具有还原性
下列说法正确的是()
| A.图a中,随着电解的进行,溶液中c(H+)增大 |
| B.图b中,Mg电极做电池负极 |
| C.图c中,发生的反应为Co+Cd2+=Cd+Co2+ |
| D.图d中,K分别与M、N连接,Fe电极均受到保护 |
一定条件下,碳钢腐蚀与溶液pH的关系如下表。下列说法不正确的是()
| pH |
2 |
4 |
6 |
6.5 |
8 |
13.5 |
14 |
| 腐蚀快慢 |
较快 |
慢 |
较快 |
||||
| 主要产物 |
Fe2+ |
Fe3O4 |
Fe2O3 |
FeO2- |
A.当溶液pH<4,碳钢主要发生析氢腐蚀
B.当溶液pH>13.5,碳钢腐蚀的正极反应式为O2+4H++4e-=2H2O
C.当溶液pH>6,碳钢主要发生吸氧腐蚀
D.煮沸除去氧气的碱性溶液中,碳钢腐蚀速率会减缓
化学反应中一定伴随着能量的变化,下列有关能量的说法正确的是()
| A.等物质的量的硫蒸气和硫粉分别完全燃烧,后者放出热量多 |
| B.由C(石墨)==C(金刚石)-1.9KJ可知,金刚石比石墨稳定 |
| C.根据热化学方程式:S(s)+O2(g)=SO2(g)+297.23kJ,可推知1molSO2(g)的能量总和大于1moS(s)和1molO2(g)的能量总和 |
| D.在稀水溶液中 H+(aq)+OH-(aq) ="=" H2O(l)+57.3 kJ,将含0.5 mol H2SO4的浓硫酸与含l mol NaOH的溶液混合时,放出的热量大于57.3 kJ |
图是反应CO(g)+2H2(g) CH3OH(g)进行过程中的能量变化曲线。曲线Ⅰ和曲线Ⅱ分
CH3OH(g)进行过程中的能量变化曲线。曲线Ⅰ和曲线Ⅱ分
别表示不使用催化剂和使用催化剂的反应过程。对该反应的下列说法正确的是()
| A.该反应的△H=+91kJ/mol |
| B.加入催化剂,该反应的△H变小 |
| C.如果该反应生成液态CH3OH,则△H变大 |
| D.反应物的总能量大于生成物的总能量 |