下列各组溶液中,不用任何其他试剂就能鉴别的是
| A.Na2SO4 H2SO4 AlCl3 BaCl2 |
| B.HCl NaOH K2SO4 NaHCO3 |
| C.NaAlO2 KHCO3 NaCl NaHSO4 |
| D.NaOH FeCl3 MgCl2 K2SO4 |
以葡萄糖为燃料的微生物燃料电池结构示意图如图所示。关于该电池的叙述正确的是( )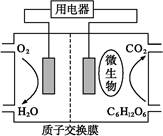
| A.该电池能够在高温下工作 |
B.电池的负极反应为:C6H12O6+6H2O-24e- 6CO2↑+24H+ 6CO2↑+24H+ |
| C.放电过程中,H+从正极区向负极区迁移 |
| D.在电池反应中,每消耗1 mol氧气,理论上能生成标准状况下CO2气体 L |
一种基于酸性燃料电池原理设计的酒精检测仪,负极上的反应为:CH3CH2OH-4e-+H2O CH3COOH+4H+。下列有关说法正确的是( )
CH3COOH+4H+。下列有关说法正确的是( )
| A.检测时,电解质溶液中的H+向负极移动 |
| B.若有0.4 mol电子转移,则在标准状况下消耗4.48 L氧气 |
C.电池反应的化学方程式为:CH3CH2OH+O2 CH3COOH+H2O CH3COOH+H2O |
D.正极上发生的反应为:O2+4e-+2H2O 4OH- 4OH- |
固体氧化物燃料电池是由美国西屋(Westinghouse)公司研制开发的。它以固体氧化锆—氧化钇为电解质,这种固体电解质在高温下允许氧离子(O2-)在其间通过。该电池的工作原理如图所示,其中多孔电极a、b均不参与电极反应。下列判断正确的是( )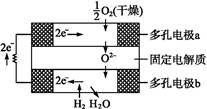
| A.有O2放电的a极为电池的负极 |
| B.有H2放电的b极为电池的正极 |
C.a极对应的电极反应为O2+2H2O+4e- 4OH- 4OH- |
D.该电池的总反应方程式为2H2+O2 2H2O 2H2O |
有四种燃料电池:
| A.固体氧化物燃料电池 | B.碱性氢氧化物燃料电池 |
| C.质子交换膜燃料电池 | D.熔融盐燃料电池, |
下面是工作原理示意图,其中正极反应生成水的是( )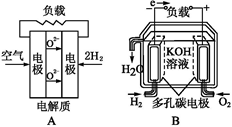
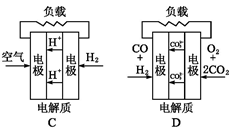
美国加州Miramar海军航空站安装了一台250 kW的MCFC型燃料电池,该电池可同时供应电和水蒸气,其工作温度为600~700 ℃,所用燃料为H2,电解质为熔融的K2CO3。该电池的总反应为2H2+O2 2H2O,负极反应为H2+C-2e-
2H2O,负极反应为H2+C-2e- H2O+CO2。则下列推断中正确的是( )
H2O+CO2。则下列推断中正确的是( )
A.正极反应:4OH--4e- 2H2O+O2↑ 2H2O+O2↑ |
| B.当电池生成1 mol H2O时,转移4 mol电子 |
| C.放电时C向负极移动 |
| D.放电时C向正极移动 |