下列物质的熔沸点高低顺序正确的是
| A.金刚石>晶体硅>二氧化硅>碳化硅 |
| B.Cl4>CBr4>CCl4>CH4 |
| C.MgO>H2O>O2>N2 |
| D.金刚石>生铁>纯铁>钠 |
对物质进行分类是化学学习中的常用方法。下列物质中属于酸的是
| A.CO | B.NaOH | C.HNO3 | D.CuSO4 |
下列物质中,其产量可以用来衡量一个国家石油化工发展水平的是
| A.甲烷 | B.乙烯 | C.苯 | D.乙醇 |
下列说法正确的是
| A.金属氧化物一定是碱性氧化物 |
| B.碱性氧化物一定是金属氧化物 |
| C.非金属氧化物一定是酸性氧化物 |
| D.酸性氧化物一定是非金属氧化物 |
滴加新制氯水后,下列各组离子可能大量存在的是
| A.Fe3+、Al3+、Cl-、NO3- | B.K+、Na+、I-、SO42- |
| C.Ag+、Ca2+、NH4+、NO3- | D.Na+、Ba2+、CO32-、SO42- |
在某无色溶液中缓慢地滴入NaOH溶液直至过量,产生沉淀的质量与加入的NaOH溶液体积的关系如图所示,由此确定,原溶液中含有的阳离子是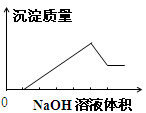
| A.Mg2+、Al3+、Fe2+ | B.H+、Mg2+、Al3+ |
| C.H+、Ba2+、Al3+ | D.只有Mg2+、Al3+ |