如图所示,试管中集满干燥的氯气,胶头滴管中装有供反应的足量浓氨水.滴入浓氨水,开始时试管内发生的反应有氧化还原反应:NH3+Cl2→N2+HCl并产生红光和白烟。
请根据以上反应和现象回答下列问题:
(1)标志反应全部完成的现象是______.
(2)反应完毕后,将试管浸入水中并倒立着试管,取下滴管,有水进入试管,在室温时,进入试管内的水约占试管容积的______。
(3)反应中生成的白烟是______。
(4)用写出试管中反应的化学方程式________。
化学与资源利用、材料研制、环境保护等密切相关。根据下列要求填写:
① 工业上制造光导纤维的基本原料是。(填化学式)
② 下列物质中,可用来制造耐火材料的是。(填字母)
| A.金刚石 | B.氧化镁 | C.三氧化二铝 | D.过氧化钠 |
③ 在生铁和钢这2种金属材料中,含碳量较高的是。
④ 在炼铁、水泥和玻璃的化学工业中,都需要的原料是。(填俗名)
⑤ 2008年北京奥运会奖牌用玉,其主要化学成分为Ca2Mg5Si8O22(OH)2,把它写成氧化物的形式为。
氮化钠(Na3N)是科学家制备的一种重要的化合物,它与水作用可产生NH3。
请回答下列问题:
(1)Na3N是由_________键形成的化合物。
(2)Na3N与盐酸反应生成__________种盐。
(3)Na3N与水的反应属于______________反应。
将一定质量的Mg、Al合金全部溶解在500mL盐酸中(体积变化不计),取10mL反应后的溶液,加1mol/L的NaOH溶液得下图关系。



(1)求Mg, Al质量各是多少?
(2)求盐酸的物质的量浓度为多少mol/L?
A、B、C、D是四种常见单质,其对应元素的原子序数依次增大,其中B、D属于常见金属,其余均为常见化合物,J是一种黑色固体,I的浓溶液具有还原性,从A—I的所有物质之间有如下的转化关系:
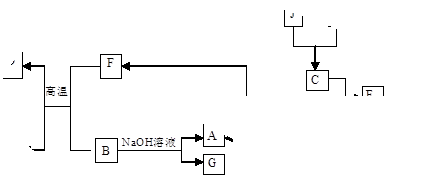
 (1)写出下列物质的名称 A;G。
(1)写出下列物质的名称 A;G。 (2)写出下列反应的化学方程式:
(2)写出下列反应的化学方程式: ①B+F→D+H:;
①B+F→D+H:; ②D→A+F:;
②D→A+F:; ③B→A+G:。
③B→A+G:。
用脱脂棉包住约0.2 g过氧化钠粉末,置于石棉网上,往脱脂棉上滴水,可观察到脱脂棉剧烈燃烧起来。
(1)由上述实验现象所得出的有关过氧化钠跟水反应的结论是:第一,有氧气生成;第二,____________。
过氧化钠跟水反应的化学方程式是________________________。
(2)某研究性学习小组拟用右图装置进行实验,以证明上述结论。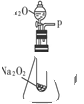
用以验证第一条结论的实验方法是:__________________。
用以验证第二条结论的实验方法及现象是:_______________________________。
(3)实验(2)中往试管内加水至固体完全溶解且不再有气泡生成后,取出试管,往试管中滴入酚酞试液,发现溶液变红;振荡后,红色褪去。为探究此现象,该小组同学查阅有关资料得知:Na2O2与H2O反应可生成H2O2,H2O2具有强氧化性和漂白性。请设计一个简单的实验,证明Na2O2和足量H2O充分反应后的溶液中有H2O2存在。现有Na2S溶液、KI溶液、红色布条等,请从中选择试剂,加以验证(只要求列出实验所用的试剂及观察到的现象)。
试剂:____________。现象:______________。