某物质的晶体中含A、B、C三种元素,其排列方式如图C的原子个数比依次为
A.1∶3∶1
B.2∶3∶1
C.2∶2∶1
D.1∶3∶3
烃①2-甲基丁烷②2,2-二甲基丙烷③戊烷④丙烷⑤丁烷,沸点由高到低顺序排列是
| A.①>②>③>④>⑤ | B.②>③>⑤>④>① |
| C.③>①>②>⑤>④ | D.④>⑤>②>①>③ |
下列叙述正确的是
| A.乙醇能发生氧化反应而乙酸不能发生氧化反应 |
| B.乙醇和乙酸之间能发生酯化反应,酯化反应和皂化反应互为逆反应 |
| C.乙烯、聚氯乙烯都能使溴水褪色 |
| D.苯、乙醇、乙酸都能发生取代反应 |
下图是用球棍模型表示的某有机反应的过程,则该反应的有机反应类型是
| A.取代反应 | B.加成反应 | C.聚合反应 | D.酯化反应 |
下列说法不正确的是
| A.O2和O3互为同素异形体 |
B. 互为同位素 互为同位素 |
C.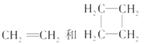 互为同系物 互为同系物 |
D. 互为同分异构体 互为同分异构体 |
下列物质属于醇类的是