对于反应2SO2+O22SO3,下列判断正确的是( )
| A.2体积SO2和足量O2反应,必定生成2体积SO3 |
| B.其他条件不变,压缩体积来增大压强,反应速率必然加快 |
| C.平衡时,SO2消耗速率必定等于O2生成速率的两倍 |
| D.平衡时,SO2浓度必定等于O2浓度的两倍 |
已知:为使Fe3+、Fe2+、Zn2+较完全的形成氢氧化物沉淀,溶液的pH应分别为3.7、9.6、4.4左右。某硫酸锌酸性溶液中含有少量Fe3+、Fe2+,为除去这些离子制得纯净的硫酸锌,应加入的试剂是( )
| A.NaOH溶液 | B.氨水 | C.KMnO4、ZnCO3 | D.H2O2、ZnO |
在下列溶液中,各组离子一定能够大量共存的是( )
| A.使酚酞试液变红的溶液: Na+、Cl—、SO42—、Fe3+ |
| B.由水电离的c(H+)=10-12 mol·L—1的溶液:K+、Ba2+、Cl—、Br— |
| C.在pH = 1溶液中:NH4+、Fe2+、NO3—、Cl— |
| D.所含溶质为Na2SO4的溶液:K+、CO32-、NO3-、Al3+ |
关于小苏打水溶液的表述正确的是()
| A.c (Na+)="c" (HCO3-) + c (CO32-) + 2c (H2CO3) |
| B.c (Na+) + c (H+) =" c" (HCO3-) + 2c (CO32-) +c (OH-) |
| C.HCO3-的电离程度大于HCO3-的水解程度 |
D.存在的电离有:NaHCO3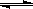 Na++HCO3—,HCO3— Na++HCO3—,HCO3—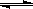 H++CO32—,H2O H++CO32—,H2O 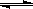 H++OH— H++OH— |
相同温度下,100mL 0.01 mol·L-1的醋酸溶液与10mL 0.1 mol·L-1的醋酸溶液相比较,下列数值前者大于后者的是()
| A.中和时所需NaOH的量 | B.c(H+) |
| C.c(OH-) | D.c(CH3COOH) |
常温下,取浓度相等的NaOH和HCl溶液,以3∶2体积比相混和,所得溶液的PH等于12,则原溶液的浓度为()
| A.0.01mol/L | B.0.017mol/L | C.0.05mol/L | D.0.50mol/L |