目前人们正在研究开发一种高能电池——钠硫电池,它是以熔融的钠、硫为两极,以Na+导电的β′Al2O3陶瓷作固体电解质,反应如下:
2Na+xS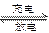 Na2Sx
Na2Sx
以下说法,正确的是( )
| A.放电时,钠作正极、硫作负极 |
| B.放电时,钠极发生还原反应 |
| C.充电时,钠极与外接电源正极相连,硫极与外接电源负极相连 |
D.充电时,阳极发生的反应是: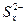  xS+2e- xS+2e- |
钢铁发生电化学腐蚀时,负极发生的反应是
| A.2H++2e-==H2 | B.2H2O+O2+4e-="=" 4OH- |
| C.Fe-2e-==Fe2+ | D.4OH-+4e-==2H2O+O2 |
下列反应不可能是原电池反应的是
| A.Fe + 2H+ = Fe2+ + H2↑ | B.H+ + OH- = H2O |
| C.2H2 + O2 = 2H2O | D.Fe2+ + Zn =" Fe" + Cu2+ |
铜片和锌片用导线连接后插入稀硫酸中,锌片是
| A.阴极 | B.正极 | C.阳极 | D.负极 |
对于加热条件下反应3Cl2+6KOH = 5KCl+KClO3+3H2O,以下叙述正确的是
| A.Cl2是氧化剂,KOH是还原剂 |
| B.被氧化的Cl原子和被还原的Cl原子的物质的量的比为5∶1 |
| C.Cl2既是氧化剂又是还原剂 |
| D.每生成1mol的KClO3转移6mol的电子 |
在氯水中存在多种分子和离子可通过实验的方法加以确定,下列说法中可能错误的是
| A.加入含有NaOH的酚酞试液,红色褪去,说明有H+存在 |
| B.加入有色布条后,有色布条褪色,说明有HClO分子存在 |
| C.氯水呈浅黄绿色,且有刺激性气味,说明有Cl2分子存在 |
| D.加入硝酸酸化的AgNO3溶液产生白色沉淀,说明有Cl-存在 |