沼气的主要成分是甲烷,沼气除可用作燃料外,还可用于制取炭黑。高温时,甲烷发生分解反应,生成乙炔和氢气,所得混合气体的密度(标准状况)是( )
| A.0.178 g·L-1 | B.0.357 g·L-1 | C.0.714 g·L-1 | D.1.43 g·L-1 |
一定温度下,三种碳酸盐MCO3(M:Mg2+、Ca2+、Mn2+)的沉淀溶解平衡曲线如图所示.已知:pM=﹣lgc(M),p(CO32﹣)=﹣lgc(CO32﹣).下列说法正确的是
| A.MgCO3、CaCO3、MnCO3的Ksp依次增大 |
| B.a 点可表示MnCO3的饱和溶液,且c(Mn2+)=c(CO32﹣) |
| C.b 点可表示CaCO3的饱和溶液,且c(Ca2+)<c(CO32﹣) |
| D.c 点可表示MgCO3的不饱和溶液,且c(Mg2+)>c(CO32﹣) |
某电源装置如图所示,电池总反应为2Ag+Cl2═2AgCl.下列说法正确的是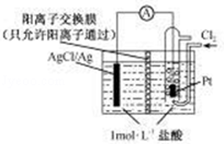
| A.正极反应为AgCl+e﹣═Ag+Cl﹣ |
| B.放电时,交换膜右侧溶液中有大量白色沉淀生成 |
| C.若用NaCl溶液代替盐酸,则电池总反应随之改变 |
| D.当电路中转移0.01mol e﹣时,交换膜左则溶液中约减少0.02mol离子 |
铜镁合金1.52g完全溶解于50mL 密度为1.40g/mL、质量分数为63%的浓硝酸中,得到NO2和N2O4的混合气体1120mL(标准状况),向反应后的溶液中加入1.0mol/L NaOH溶液,当金属离子全部沉淀时,得到2.54g沉淀.下列说法不正确的是
| A.该合金中铜与镁的物质的量之比是2:1 |
| B.该浓硝酸中HNO3的物质的量浓度是14.0 mol/L |
| C.NO2和N2O4的混合气体中,NO2的体积分数是80% |
| D.得到2.54 g沉淀时,加入NaOH溶液的体积是600 mL |
25℃时,在10mL浓度均为0.1mol/L的NaOH和NH3•H2O混合溶液中滴加0.1mol•L﹣1盐酸,下列有关溶液中粒子浓度关系正确的是
| A.未加盐酸时:c(OH﹣)>c(Na+)=c(NH3•H2O) |
| B.加入10mL盐酸时:c(NH4+)+c(H+)=c(OH﹣) |
| C.加入盐酸至溶液pH=7时:c(Cl﹣)=c(Na+) |
| D.加入20mL盐酸时:c(Cl﹣)=c(NH4+)+c(Na+) |
有关下图所示化合物的说法不正确的是 
| A.既可以与Br2的CCl4溶液发生加成反应,又可以在光照下与Br2发生取代反应 |
| B.1mol该化合物最多可以与3molNaOH反应 |
| C.既可以催化加氢,又可以使酸性KMnO4溶液褪色 |
| D.既可以与FeCl3溶液发生显色反应,又可以与NaHCO3溶液反应放出CO2气体 |