钠玻璃中Na2O、CaO、SiO2三者的物质的量之比为1∶1∶6,则钠玻璃中Na2SiO3、CaSiO3、SiO2的物质的量之比为( )
| A.1∶1∶6 | B.2∶1∶6 | C.1∶1∶4 | D.2∶1∶4 |
下列离子方程式书写正确的是:()
A.硫酸亚铁加过氧化氢溶液:Fe2+ + H2O2 + 2H+ Fe3+ + 4H2O
Fe3+ + 4H2O
B.将少量硝酸银溶液滴入氨水中:Ag+ + 2NH3·H2O [Ag(NH3)2]+ + 2H2O
[Ag(NH3)2]+ + 2H2O
C.KAl(SO4)2中滴加Ba(OH)2使SO42-恰好完全沉淀:
2Al3++3 SO42-+3 Ba2++6 OH-=2Al(OH)3↓+3BaSO4↓
D铝粉与NaOH的溶液反应:2Al + 2OH- AlO2-+ H2↑
AlO2-+ H2↑
下列反应的离子方程式书写正确的是( )
| A.碳酸钡溶于醋酸溶液:BaCO3+2H+=Ba2++CO2↑+H2O |
| B.向氯化铝溶液中加入过量氨水:Al3++3NH3·H2O=Al(OH)3↓+3NH4+ |
| C.在三氯化铁的酸性溶液中通入足量的硫化氢:Fe3++H2S=Fe2++S↓+2H+ |
| D.向饱和碳酸氢钙溶液中加入过量的NaOH溶液:Ca2++HCO3-+OH-=CaCO3↓+H2O |
下列各组离子能在指定溶液中,大量共存的是:( )
①无色溶液中:K+,Cl—,Na+,MnO4—,NO3—,SO42—
②使PH=11的溶液中:CO32—,Na+,AlO2—,NO3—,S2—,SO32—
③水电离的H+浓度C(H+)=10—12mol·L—1的溶液中:Cl—,HCO3—,NO3—,NH4+,S2O32—
④加入Mg能放出H2的溶液中:Mg2+,NH4+,Cl—,K+,SO42—
⑤使甲基橙变红的溶液中:Fe3+,MnO4—,NO3—,Na+,SO42—
⑥酸性溶液中:Fe2+,Al3+,NO3—,I—,Cl—,S2—
A①②⑤ B①③⑥ C②④⑤ D①②④
下列说法或表示方法正确的是( )
| A.等物质的量的硫蒸气和硫固体分别完全燃烧,后者放出热量多 |
| B.由C(石墨)= C(金刚石);△H =" +1.90" kJ·mol-1可知,金刚石比石墨稳定 |
| C.在稀溶液中,H+(aq)+ OH-(aq)= H2O(l);△H =" -57.3" kJ·mol-1,若将含0.5 mol H2SO4的浓硫酸与含1 mol NaOH的溶液混合,放出的热大于57.3 kJ |
| D.在101 kPa时,2 g H2完全燃烧生成液态水,放出285.8 kJ热量,氢气燃烧的热化学方程式表示为:2H2(g)+ O2(g)= 2H2O(l);△H =" -285.8" kJ·mol-1 |
2008年北京奥运会“祥云”火炬用的是环保型燃料——丙烷(C3H8),悉尼奥运会火炬所用燃料为65%丁烷(C4H10)和35%丙烷,已知丙烷的燃烧热为: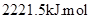 -1,下列有关说法正确的是()
-1,下列有关说法正确的是()
| A.奥运火炬燃烧主要是将化学能转变为热能和光能 |
| B.丙烷的沸点比正丁烷高 |
| C.丙烷、空气及铂片可组成燃料电池,在丙烷附近的铂极为电池的正极 |
| D.丙烷燃烧的热化学方程式为C3H8(g)+5O2(g)=3CO2(g)+4H2O(g);△H=-2221.5kJ/mol |