有一无色溶液,可能含有K+、Al3+、Mg2+、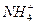 、Cl-、
、Cl-、 、
、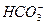 、
、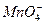 中的一种或几种。为确定其成分,做如下实验:①取部分溶液,加入适量Na2O2固体产生无色无味的气体并生成白色沉淀,再加入足量的NaOH溶液后白色沉淀部分溶解;②另取部分溶液,加入HNO3酸化的Ba(NO3)2溶液,有白色沉淀产生。下列推断正确的是( )
中的一种或几种。为确定其成分,做如下实验:①取部分溶液,加入适量Na2O2固体产生无色无味的气体并生成白色沉淀,再加入足量的NaOH溶液后白色沉淀部分溶解;②另取部分溶液,加入HNO3酸化的Ba(NO3)2溶液,有白色沉淀产生。下列推断正确的是( )
A.肯定有K+、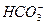 、 、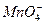 |
B.肯定有Al3+、Mg2+、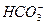 |
C.肯定有Al3+、Mg2+、 |
D.肯定有Al3+、Mg2+、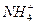 、Cl- 、Cl- |
用NA表示阿伏加德罗常数的值。下列叙述正确的是
| A.标准状况下,13g苯和苯乙烯混合物中含有NA个C-H键 |
| B.25℃时,pH =12的氨水中含有0.01NA个NH4+与NH3·H2O |
| C.t℃时,28g CO、C2H4混合气体,所占的体积为22.4 L |
| D.室温下,27g铝投入100 mL6mol·L-1的NaOH溶液中,转移3 NA个电子 |
物质A~E的转化关系如图所示:
已知气体单质D能使带火星的木条复燃,反应①是实验室制单质D的常用方法之一,反应②是实验室制黄绿色气体E的重要反应,(部分生成物未列出)。
依据上述信息,回答下列问题:
(1)A的化学式
(2) 从氯元素化合价的变化看,以上写出反应②③④⑤四种方法的共同点是
(3)写出反应④的化学方程式
(4)利用反应③④⑤的变化,不写化学方程式比较A、C、D的氧化性由大到小的顺序
(5)写出反应②的离子方程式,氧化剂与还原剂的物质的量之比
某同学设计了一种用电解法制取某些物质的通用实验装置(如右图)。下列说法中不正确的是
| A.如果用于制Fe(OH)2且装置中是氯化钠溶液,电源中“a”为正极,“ b”为负极 |
| B.如果用于制Fe(OH)2且装置中是氯化钠溶液,则A的电极材料应为铁,而B电极可用某一导电物质如石墨 |
| C.如果用于制漂白液,且装置中是氯化钠溶液,电源中“a”为正极,“ b”为负极 |
| D.如果用于制漂白液,且装置中是氯化钠溶液,电源中“b”电极材料一定不能为铁 |
常温时,将500 ml pH=a的CuSO4和K2SO4的混合溶液用石墨电极电解一段时间,测得溶液的pH变为b(假设溶液体积的变化忽略不计),在整个电解过程中始终发现只有一个电极有气体产生。下列说法错误的是()
| A.若使溶液恢复到电解前的浓度可以向溶液中加20(10-b-10-a)g CuCO3 |
| B.b<a<7 |
| C.阳极电极反应:2H2O—4e—=O2↑+4H+ |
| D.整个过程中是阳极产生氧气,阴极析出铜单质 |
某溶液中只含有Na+、H+、OH-、A-四种离子,下列说法不正确的是()
A.此溶液中的溶质有可能是一种,也可能是两种
B.溶液中可能存在:c(Na+)> c(OH-) >c(H+) > c (A-)
C.溶液中可能存在:c(Na+)> c(A-) > c(OH-)>c(H+)
D.若溶质为NaA、NaOH,则一定存在:c(Na+) > c(A-) > c(OH-)> c(H+)