下列实验现象,与新制氯水中的某些成分(括号内物质)没有关系的是
| A.将NaHCO3固体加入新制氯水,有无色气泡(H+) |
| B.使红色布条褪色(HCl) |
| C.向FeCl2溶液中滴加氯水,再滴加KSCN溶液,发现呈血红色(Cl2) |
| D.滴加AgNO3溶液生成白色沉淀(Cl-) |
根据下列化学方程式,判断有关物质的还原性强弱的顺序为
① I2+SO2+2H2O=H2SO4+2HI;
② 2FeCl2+Cl2=2FeCl3;
③ 2FeCl3+2HI=2FeCl2+2HCl+I2
| A.I->Fe2+>Cl->SO2 | B.SO2>I->Fe2+>Cl- |
| C.Fe2+>I->Cl->SO2 | D.Cl->Fe2+>SO2>I- |
下列离子方程式改写成化学方程式正确的是
| A.Cu2++2OH-=Cu(OH)2¯ CuCO3+2NaOH=Cu(OH)2¯+Na2CO3 |
B.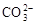 +2H+=CO2+H2O BaCO3+2HCl=BaCl2+CO2+H2O +2H+=CO2+H2O BaCO3+2HCl=BaCl2+CO2+H2O |
C.Ca2++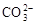 =CaCO3¯Ca(NO3)2+Na2CO3=CaCO3¯+2NaNO3 =CaCO3¯Ca(NO3)2+Na2CO3=CaCO3¯+2NaNO3 |
| D.H++OH-=H2O Ba(OH)2+H2SO4=BaSO4 ¯+2H2O |
在水溶液中能大量共存,且加入过量稀硫酸溶液时,有气体生成的是
| A.Na+、Ag+、CO32- 、Cl- | B.K+ 、Ba2+ 、SO42- 、Cl- |
| C.Na+、K+、CO32- 、Cl- | D.Na+ 、K+ 、Cl-、SO42— |
硫酸钾和硫酸铝的混合溶液,已知其中Al3+的浓度为0.4 mol/L,硫酸根离子浓度为0.7 mol/L,则K+的物质的量浓度为
| A.0.1 mol/L | B.0.2 mol/L | C.0.3 mol/L | D.0.15 mol/L |
某一化学兴趣小组的同学在家中进行实验,按照图示连接好线路,发现图B中的灯泡亮了。由此得出的以下结论中正确的是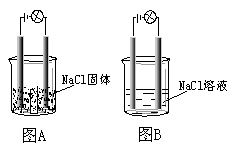
| A.NaCl是非电解质 |
| B.NaCl溶液是电解质 |
| C.NaCl在水溶液中电离出了可以自由移动的离子 |
| D.在NaCl溶液中,水电离出了大量的离子 |