用酸性氢氧燃料电池为电源进行电解的实验装置示意图如下图所示。下列说法中,正确的是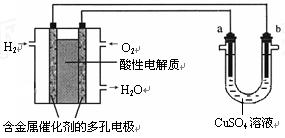
| A.燃料电池工作时,正极反应为:O2 + 2H2O + 4e-=4OH- |
| B.a极是铁,b极是铜时,b极逐渐溶解,a极上有铜析出 |
| C.a极是粗铜,b极是纯铜时,a极逐渐溶解,b极上有铜析出 |
| D.a、b两极均是石墨时,在相同条件下a极产生的气体与电池中消耗的H2体积相等 |
下列化学方程式书写正确的是
A.P + O2 P2O5 P2O5 |
B.4Fe + 3O2 2Fe2O3 2Fe2O3 |
C.2KMnO4 K2MnO4 + MnO2 +O2↑ K2MnO4 + MnO2 +O2↑ |
| D.2Fe+3H2SO4═Fe2(SO4)3+H2↑ |
用分子的相关知识解释下列生活中的现象,其中错误的是
| A.非吸烟者受到被动吸烟的危害,是因为分子在不断地运动 |
| B.热胀冷缩,说明分子的大小随温度升降而改变 |
| C.10mL酒精和10mL水混合后体积小于20mL,说明分子间有间隔 |
| D.不同的花儿有不同的香味,是因为不同的分子性质不同 |
决定元素种类的是
| A.电子数 | B.质子数 | C.中子数 | D.最外层电子数 |
下列图示的基本实验操作中,正确的是
下列有关物质变化的说法错误的是
| A.粉笔写字的过程是物理变化 |
| B.在化学变化中,原子可以变成其他原子 |
| C.在化学变化中,分子可以变成其他分子 |
| D.在化学变化中伴随着能量变化 |