下列物质中,含有非极性共价键的是
| A.N2 | B.CO2 | C.NaOH | D.CH4 |
原电池产生电流的本质原因是
| A.原电池中溶液能电离出自由移动的离子 |
| B.有导线将两个活动性不同的电极连接 |
| C.正极发生了还原反应,负极发生了氧化反应 |
| D.电极上进行的氧化还原反应中有电子的转移 |
X元素最高价氧化物对应的水化物为H3XO4,则它对应的气态氢化物为
| A.HX | B.H2X | C.XH4 | D.XH3 |
在2A+B 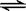 3C+4D中,表示该反应速率最快的是
3C+4D中,表示该反应速率最快的是
A.υ(A) = 0.5mol/(L·s) B.υ(B) =" 0.3" mol/(L·s)
C.υ(C) = 0.8mol/(L·s)D.υ(D)=" 1" mol/(L·s)
根据元素在周期表中的位置判断,下列元素中原子半径最小的是
| A.氧 | B.氟 | C.碳 | D.氮 |