ClSO3H称之为氯磺酸,是一种强酸,它和甲酸能发生如下反应:HCOOH+ClSO3H CO+HCl+H2SO4,以下判断正确的是( )
CO+HCl+H2SO4,以下判断正确的是( )
| A.反应属氧化还原反应 | B.反应属非氧化还原反应 |
| C.反应后溶液的pH减小 | D.反应后溶液的pH增大 |
(10分)X、Y、Z、W是元素周期表前四周期中的四种常见元素,其相关信息如下表:
| 元素 |
相关信息 |
| X |
X的基态原子核外3个能级上有电子,且每个能级上的电子数相等 |
| Y |
Y元素的激发态原子的电子排布式为1s22s22p63s23p34s1 |
| Z |
Z和Y同周期,Z的电负性大于Y |
| W |
W的一种核素的质量数为63,中子数为34 |
(1)Y离子半径Z离子半径(选填“>”、“=”、“<”)。
(2)XY2是一种常用的溶剂,一个XY2的分子中存在个σ键,____________个π键。
(3)在H―Y、H―Z两种共价键中,键的极性较强的是,键长较长的是。
(4)向WYO4的水溶液中逐滴加入氨水至过量,观察到溶液由天蓝色最终变为色。反应过程中涉及的离子方程式为:、。
已知磷酸分子 中的三个氢原子都可以跟重水分子(D2O)中的D原子发生氢交换,又知次磷酸(H3PO2)也可跟D2O进行氢交换,但次磷酸钠(NaH2PO2)却不再能跟D2O发生氢交换,由此可推断出H3PO2的分子结构是
中的三个氢原子都可以跟重水分子(D2O)中的D原子发生氢交换,又知次磷酸(H3PO2)也可跟D2O进行氢交换,但次磷酸钠(NaH2PO2)却不再能跟D2O发生氢交换,由此可推断出H3PO2的分子结构是
下图中每条折线表示周期表ⅣA~ⅦA中的某一族元素氢化物的沸点变化。每个小黑点代表一种氢化物,其中a点代表的是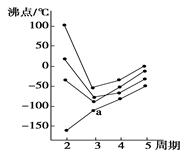
| A.H2S | B.HCl | C.PH3 | D.SiH4 |
碘单质在水溶液中溶解度很小,但在CCl4中溶解度很大,这是因为
| A.CCl4与I2都是直线型分子,而H2O不是直线型分子 |
| B.CCl4与I2分子量相差较小,而H2O与I2分子量相差较大 |
| C.CCl4和I2都不含氢元素,而H2O中含有氢元素 |
| D.CCl4和I2都是非极性分子,而H2O是极性分子 |
下列说法正确的是
| A.氢键有方向性和饱和性,属于共价键 |
| B.H2O是一种非常稳定的化合物,这是由于氢键所致 |
| C.范德华力是一种分子间作用力,也是一种特殊的化学键 |
| D.常温常压下,卤素单质从F2→I2由气态、液态到固态的原因是范德华力逐渐增大 |