下列实验事实不能证明醋酸是弱酸的是
| A.常温下,测得醋酸钠溶液的pH>7 |
| B.常温下,测得0.1mol/L醋酸溶液的pH=4 |
| C.常温下,将pH=1的醋酸溶液稀释1000倍,测得pH<4 |
| D.常温下,将物质的量浓度相同的醋酸溶液与氢氧化钠溶液等体积混合后恰好中和 |
下列关于实验现象的描述不正确的是
| A.把铜片和铁片紧靠在一起浸入稀硫酸中,铜片表面出现气泡 |
| B.用锌片做阳极,铁片做阴极,电解氯化锌溶液,铁片表面出现一层锌 |
| C.把铜片插入三氯化铁溶液中,在铜片表面出现一层铁 |
| D.把锌粒放入盛有盐酸的试管中,加入几滴氯化铜溶液,气泡放出速率加快 |
关于如图所示装置的叙述,正确的是
| A.铜是阳极,铜片上有气泡产生 |
| B.铜片质量逐渐减少 |
| C.电流从锌片经导线流向铜片 |
| D.氢离子在铜片表面被还原 |
下列各组在溶液中的反应,无论反应物的量多少,都能用同一离子方程式表示的是
| A.Ba(OH)2与H2SO4 | B.FeBr2与Cl2 |
| C.HCl与Na2CO3 | D.NaHCO3与Ca(OH)2 |
下列离子方程式正确的是
| A.向漂白粉溶液中通入少量二氧化硫:Ca2++2ClO-+SO2+H2O=CaSO3↓+2HClO |
B.稀硝酸中加入过量铁粉:Fe+4H++NO =Fe3++NO↑+2H2O =Fe3++NO↑+2H2O |
| C.溴化亚铁溶液中通入足量氯气:2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl- |
D.苯酚钠溶液中通入少量二氧化碳: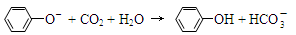 |
还原2.4×10-3mol XO(OH)3+ 到X元素的低价态时,需消耗30mL0.2mol· 的亚硫酸钠溶液,则在此反应中X元素的低价态为
的亚硫酸钠溶液,则在此反应中X元素的低价态为
| A.0价 | B.+1价 | C.-1价 | D.-2价 |