有两只密闭容器A和B,A容器有一个移动的活塞能使容器内保持恒压,B容器能保持恒容。起始时向这两只容器中分别充入等量的体积比为2∶1的SO2与O2的混和气体,并使A和B容积相等(见下图)在保持400℃的条件下使之发生如下反应: 2SO2+O2 2SO3(气)
2SO3(气) 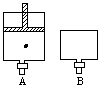
(1)达到平衡时所需的时间A容器比B容器____,A容器中SO2的转化率比B容器_____。
(2)达到(1)所述平衡后,若向两容器中通入等量的氩气,A容器化学平衡___移动,B容器化学平衡____移动
(3)达到(1)所述平衡后,若向两容器中通入等量的原反应气体,达到新平衡时:A容器中SO3的百分含量____(增大、减小、不变。下同),B容器中SO3的百分含量____。
①~⑨是几种有机物的名称、分子式或结构简式:
①C2H2 ② 新戊烷③苯 ④ ⑤
⑤
⑥CH3CH(C2H5)CH2CH(C2H5)CH3⑦C5H10 ⑧ClCH=CHCl ⑨C5H4
据此回答下列问题:
(1)上述有机物中,互为同系物的是___________(填序号),存在顺反异构的是___________(填序号)。
(2)④与等物质的量的H2发生l,4 加成,写出所得产物的名称:_____________。
(3)请写出下列相关化学反应方程式
实验室制①:__________________。
氯气与③用氯化铁作催化剂的反应:___________________。
(4)③的同系物A,分子中共含66个电子,A苯环上一溴代物只有一种,请写出A 的结构简式____________。
(5)某烃B含氢14.3%,且分子中所有氢完全等效,向80g含Br25%的溴水中加入该有机物,溴水刚好完全褪色,此时液体总质量82.1g。则B的结构简式为:___________。
(6)⑨理论上同分异构体的数目可能有30多种。如:
| A.CH2=C=C=C=CH2 | B.CH≡C-CH=C=CH2 |
C. |
D. e. e. |
请不要顾忌这些结构能否稳定存在,其中a、b是链状分子,写出所有碳原子均共线的链状分子的结构简式:________________。若该烃的等效氢只有一种,则满足条件的异构体除a、c外还有________(只需答出一例的结构简式)。
NaHCO3是一种酸式盐,其水溶液显碱性,是重要的化工产品和化学试剂。
(1)NaHCO3俗称 ,其水溶液显碱性的原因是(用离子方程式表示) 。
(2)工业上制备NaHCO3的方法是:先向饱和食盐水通入足量的NH3,再通入过量的CO2得到NaHCO3沉淀,写出该反应的化学方程式___________________________。
(3)泡沫灭火器内含一定浓度的NaHCO3(置于铁桶内)和Al2(SO4)3溶液(置于玻璃瓶内)以及起泡剂,使用时把灭火器倒置即有泡沫状物质喷出。
①倒置灭火器时发生反应的离子方程式是___________________________;
②有人认为Na2CO3价格便宜,建议用等物质的量浓度、等体积的Na2CO3溶液代替NaHCO3溶液。你认为此建议_______(填“合理” 或“不合理”),理由是__________________。
(4)由NaHCO3和KHCO3组成的混合物,与50mL等浓度的盐酸分别反应,测得如下数据:
| 50mL盐酸 |
50mL盐酸 |
50mL盐酸 |
|
| m(混合物) |
9.2 g |
15.7 g |
27.6 g |
| V(CO2)(标况) |
2.24 L |
3.36 L |
3.36 L |
①该混合物中NaHCO3的物质的量分数为 ;
②所用盐酸的物质的量浓度是 mol·L-1。
H2O2是重要的化学试剂,在实验室和生产实际中应用广泛。
(1)写出H2O2在MnO2催化下分解的化学方式 。
(2)在“海带提碘”的实验中,利用酸性H2O2得到碘单质的离子方程式是 。
(3)实验室使用酸性KMnO4标准液测定溶液中H2O2的浓度。
①酸性KMnO4溶液应盛放在__________(填“酸式”或“碱式”)滴定管中,判断到达滴定终点的现象是 。
②完成并配平离子方程式:□MnO4-+□H2O2+□H+ = □Mn2++□O2↑+□ ,在反应中H2O2作 剂(填“氧化”或“还原”),每生成1mol O2,转移电子 mol。
已知25 ℃时有关弱酸的电离平衡常数:
| 弱酸化学式 |
HSCN |
CH3COOH |
HCN |
H2CO3 |
| 电离平衡常数 |
1.3×10—1 |
1.8×10—5 |
4.9×10—10 |
K1=4.3×10—7 K2=5.6×10—11 |
(1)同温度下,等pH值的a.NaHCO3 b.NaCN c.Na2CO3溶液的物质的量浓度由大到小的顺序为_____________(填序号)。
(2)25℃时,将20mL 0.1mol·L-1 CH3COOH溶液和20mL 0.1mol·L-1 HSCN溶液分别与20mL 0.1 mol·L-1 NaHCO3溶液混合,实验测得产生的气体体积(V)随时间(t)的变化如图所示: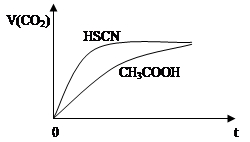
反应初始阶段两种溶液产生CO2气体的速率存在明显差异的原因是:_______________。反应结束后所得两溶液中,c(SCN—) c(CH3COO—)(填“>”、“<”或“=”)
(3)若保持温度不变,在醋酸溶液中加入一定量氨气,下列量会变小的是________(填序号)
a.c(CH3COO-) b.c(H+) c.KW d.醋酸电离平衡常数
(1)分别用等体积的蒸馏水和0.01mol/L硫酸洗涤BaSO4沉淀,用水洗涤造成BaSO4的损失量大于用稀硫酸洗涤的损失量。原因是
(请结合平衡移动原理,用相关的化学用语及文字表述回答。)
(2)Cr(OH)3在溶液中存在以下沉淀溶解平衡:Cr(OH)3(s) Cr3+(aq)+3OH-(aq),常温下,Cr(OH)3的溶度积Ksp=10-32,要使c(Cr3+)降至10-5 mol/L时,溶液的pH应调至
Cr3+(aq)+3OH-(aq),常温下,Cr(OH)3的溶度积Ksp=10-32,要使c(Cr3+)降至10-5 mol/L时,溶液的pH应调至
(3)实验证明,多元弱酸的分步电离一步比一步困难。原因是
(提示:可以从粒子的电荷情况和电离平衡的移动两方面加以考虑)
(4)在25℃下,将a mol·L-1的氨水与0.01 mol·L-1的盐酸等体积混合,反应平衡时溶液中c(NH4+)=c(Cl-),则溶液是 (填“酸”、“碱”或“中”)性;用含a的代数式表示NH3·H2O的电离常数Kb=