下列叙述中正确的是
| A.碳的摩尔质量为12g | B.摩尔是物质的质量的单位 |
| C.一个碳原子的质量为12g | D.阿伏加德罗常数约为6.02×1023mol-1 |
甲、乙、丙三种物质均含有铝元素,在溶液中的转化关系如图所示。下列说法正确的是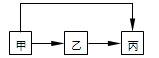
| A.若甲是Al,丙是Al(NO3)3,则乙一定是NaAlO2 |
| B.若甲是Al2O3,丙是NaAlO2,则乙一定是Al(NO3)3 |
| C.若甲是Al(NO3)3,丙是NaAlO2,则乙一定是Al(OH)3 |
| D.若甲是Al(OH)3,丙是Al(NO3)3,则乙一定是NaAlO2 |
N2O5是一种新型硝化剂,在一定温度下可发生以下反应:2N2O5(g)  4NO2(g)+O2(g)-Q(Q>0)一定温度时,向密闭容器中通入N2O5,部分实验数据见下表:
4NO2(g)+O2(g)-Q(Q>0)一定温度时,向密闭容器中通入N2O5,部分实验数据见下表:
| 时间/s |
0 |
500 |
1000 |
1500 |
| c(N2O5)/mol/L |
0.50 |
0.35 |
0.25 |
0.25 |
下列说法中错误的是
A.500 s时O2的浓度为0.075 mol/L
B.平衡后,升高温度,正反应速率先增大后减小
C.平衡后,要使平衡常数增大,改变的条件是升高温度
D.1000 s时将容器的体积缩小一半,重新达到平衡时0.25 mol/L<c(N2O5)<0.50 mol/L
常温下,将一定量的氯气通入100 mL 4 mol/L的氢氧化钠溶液中,发生反应的化学方程式为:Cl2+2NaOH → NaCl+NaClO+H2O。充分反应后,下列说法正确的是(NA为阿伏加德罗常数)
| A.当通入的Cl2为2.24 L时,反应中电子转移数目为0.1 NA |
| B.当溶液中Na+为0.4 NA时,溶液中的Cl-为0.2 NA |
| C.当电子转移数目为0.2 NA时,溶液质量增加14.2 g |
| D.当溶液质量增加7.1 g时,溶液中ClO-为0.1 NA |
为探究雾霾颗粒中的可溶性成分,某课外活动小组采集雾霾颗粒样品,用蒸馏水浸取得到浸取液,取浸取液进行以下实验,其中根据实验现象得出的结论正确的是
| A.滴入NaOH溶液,有白色沉淀产生,说明雾霾中一定含Mg2+ |
| B.滴入AgNO3溶液,有白色沉淀产生,说明雾霾中一定含Cl― |
| C.滴入硝酸酸化的BaCl2溶液,有白色沉淀产生,说明雾霾中一定含SO42― |
| D.加入浓NaOH溶液微热,试管口的湿润红色石蕊试纸变蓝,说明雾霾中一定含NH4+ |
下表为三种元素的性质或结构信息:
| 元素编号 |
元素性质或结构 |
| X |
3p亚层上有1个空轨道 |
| Y |
第三周期元素形成的简单离子中半径最大 |
| Z |
短周期中原子最容易失电子 |
下列推断正确的是
A.氢化物的稳定性:X<Y B.单质与水反应的难易程度:Y>Z
C.单质的熔点:X<Y<Z D.X、Y、Z的氧化物晶体类型相同