镁/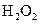 酸性燃料电池采用海水作电解质(加入一定量的酸),下列说法正确的是
酸性燃料电池采用海水作电解质(加入一定量的酸),下列说法正确的是
A.电池总反应的离子方程式为: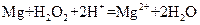 |
B.负极的电极反应为: |
| C.工作时,正极周围海水的pH减小 |
D.电池工作时,溶液中的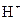 向负极移动 向负极移动 |
在0.1 mol·L-1CH3COOH溶液中存在如下电离平衡:CH3COOH  CH3COO- +H+,对于该平衡,下列叙述不正确的是
CH3COO- +H+,对于该平衡,下列叙述不正确的是
| A.加水稀释,电离平衡正向移动,溶液中n(H+)减小 |
| B.加热,电离平衡正向移动,溶液中c(CH3COO-)增大 |
| C.通入少量HCl气体,电离平衡逆向移动,溶液中c(H+)减小 |
| D.加入少量CH3COONa固体,电离平衡逆向移动,溶液中c(H+)减小 |
已知I2+SO32-+H2O==2I-+SO42-+2H+。某无色溶液中可能含有I-、NH4+、Cu2+、SO32-,向该溶液中加入少量溴水,溶液仍呈无色,则下列关于溶液的判断正确的是
①肯定不含I-②肯定不含Cu2+
③肯定含有SO32-④可能含有I-
| A.②③④ | B.①②③ | C.①③ | D.①② |
下列溶液加热蒸干灼烧后,能得到该溶质固体的是
| A.Al2(SO4)3 | B.NaHCO3 |
| C.Fe(NO3)3 | D.NH4Cl |
在25 ℃时,用0.125 mol/L的标准盐酸滴定25.00 mL未知浓度的NaOH溶液所得滴定曲线如图所示,图中K点代表的pH为
| A.13 | B.12 | C.10 | D.11 |
对于难溶盐MX,其饱和溶液中M+和X-的物质的量浓度之间的关系类似于c(H+)·c(OH-)=Kw,存在等式c(M+)·c(X-)=Ksp。现将足量的AgCl分别放入下列物质中,AgCl的溶解度由大到小的排列顺序是
①30 mL0.03 mol·L-1 AgNO3溶液②30 mL 0.02mol·L-1CaCl2溶液
③30 mL 0.03mol·L-1HI溶液④30 mL蒸馏水
| A.①>②>③>④ | B.③>④>①>② |
| C.②>①④>>③ | D.④>③>②>① |