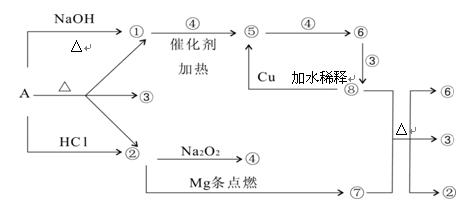
正盐A能发生下图所示的反应,图中①~⑧分别代表有关反应中的一种物质(某些物质已略去),其中①、②、④、⑤为无色气体。
请完成下列各题:
(1)写出化学式A ⑥ ⑦
(2)写出下列反应方程式:
⑧+⑦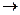 ②+③+⑥:
②+③+⑥:
①+④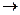 ⑤:
⑤:
(3)⑧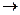 ⑤的离子方程式为:
⑤的离子方程式为:
J、L、M、R、T是原子序数依次增大的短周期主族元素,J、R在周期表中的相对位置如右表;J元素最低负化合价的绝对值与其原子最外层电子数相等;M是地壳中含量最多的金属元素。
(1)M的离子结构示意图为_____;元素T在周期表中位于第_____周期第_____族。
(2)J和氢组成的化合物分子有6个原子,其结构简式为。
(3)M和T形成的化合物在潮湿的空气中冒白色烟雾,反应的化学方程式为。
已知有以下物质相互转化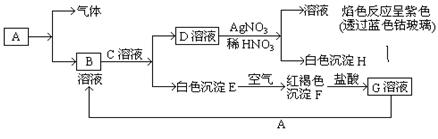
试回答:(1)写出B的化学式D的化学式。
(2)写出由E转变成F的化学方程式。
(3)写出用KSCN鉴别G溶液的离子方程式;
向G溶液加入A的有关离子反应方程式。
| J |
||||
| R |
过硫酸钾(K2S2O8)的氧化性强于KMnO4,某反应在银离子催化下可发生,该反应体系中的物质有:K2S2O8、、KMnO4、K2SO4 、 MnSO4、H2SO4、 H2O。
(1)请写出并配平上述反应的化学方程式:
(2)反应中被还原的物质是:;还原剂是:。
(6分)按要求写热化学方程式:
(1)已知稀溶液中,1 mol H2SO4与NaOH溶液恰好完全反应时,放出114.6 kJ热量,写出表示H2SO4与NaOH反应的中和热的热化学方程式__________________
(2)25℃、101 kPa条件下充分燃烧一定量的丁烷气体放出热量为Q kJ,经测定,将生成的CO2通入足量澄清石灰水中产生25 g白色沉淀,写出表示丁烷燃烧热的热化学方程式_________________________
离子化合物M(化学式为NaN3)在汽车安全气囊中有重要的作用,M与其他物质的转化关系如下图所示。已知:常温下G为淡黄色固体,H为一种常见的液体,A、B、C、X为单质,其中A、C、X为气体,A、X分别为空气的主要成分之一。I、J为常见的工业原料。相关转化关系如图所示:☆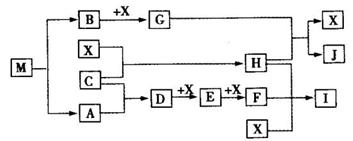
(1)实验室中物质I应如何保存?。
(2)写出D与X反应的化学方程式。
(3)G,F均能氧化SO2 ,若前一反应仅生成一种盐,后一反应生成两种氧化物,写出相应化学方程式;。
(4)常温下M受撞击时可分解,13gM完全分解为A和B时,放出a kJ的热量,写出M分解的热化学方程式。
(5)M是一种易溶于水的盐,其水溶液显弱碱性,用离子方程式解释原因。
(6)相同条件下,等体积等物质的量浓度的M溶液和NaCl溶液中,阴、阳离子总数的关系是前者后者.(填大于、等于或小于)