代表阿伏加德罗常数。下列有关叙述正确的是( )
| A. | 标准状况下,2.24 含有的分子数等于0.1 |
| B. | 常温下, 溶液中阴离子总数大于0.1 |
| C. | 分子数为 的 、 混合气体体积约为22.4 ,质量为28 |
| D. | 3.4 中含 键数目为 |
下列各组离子,在溶液中可以大量共存的是
| A.Na+、S2-、K+、SO32- | B.Na+、SO32-、H+、NO3- |
| C.NH4+、K+、Cl-、OH- | D.H+、K+、ClO-、SiO32- |
相同状况下,在容积相同的三个烧瓶内,分别充满干燥的NH3、HCl与空气1:1的混合气体、NO2气体.然后分别做喷泉实验,实验结束后,烧瓶内3种溶液的物质的量浓度之比为(假设溶质不向外扩散)
| A.3:3:2: | B.1:1:1: | C.2:2:3: | D.无法比较 |
用下图所示实验装置(夹持仪器已略去)探究铜丝与过量浓硫酸的反应。下列实验
不合理的是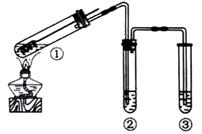
| A.③中选用NaOH溶液吸收多余的SO2 |
| B.上下移动①中铜丝可控制SO2的量 |
| C.②中选用品红溶液验证SO2的生成 |
| D.为确认CuSO4生成,向①中加水,观察颜色 |
下表所列各组物质中,不能通过一步反应实现如图所示转化的是
| 物质 选项 |
a |
b |
c |
|
|
把少量NO2气体通入过量小苏打溶液中,再使逸出的气体通过装有足量的过氧化钠颗粒的干燥管,最后收集到的气体是
| A.氧气 | B.二氧化氮 | C.二氧化氮和氧气 | D.二氧化氮和一氧化氮 |