常温下,下列溶液中的微粒浓度关系正确的是( )
| A.新制氯水中加入固体NaOH:c(Na+)=c(Cl-)+c(ClO-)+c(OH-) |
| B.pH=8.3的NaHCO3溶液:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3) |
| C.常温下,pH=7的NH4Cl与氨水的混合溶液中:c(Cl-)=c(NH4+)>c(OH-)=c(H+) |
| D.0.1 mol·L-1CH3COONa溶液中:c(OH-)=c(CH3COOH)+c(H+) |
短周期金属元素甲~丁在元素周期表中的相对位置如表所示: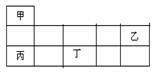
下列判断正确的是( )
| A.原子半径:丙>丁>乙 |
| B.单质的还原性:丁>丙>甲 |
| C.甲、乙、丙的氧化物均为共价化合物 |
| D.乙、丙、丁的最高价氧化物对应的水化物能相互反应 |
下列陈述Ⅰ、Ⅱ正确并且有因果关系的是( )
| 选项 |
陈述Ⅰ |
陈述Ⅱ |
| A |
向Na2O2的水溶液中滴入酚酞变红色 |
Na2O2与水反应生成氢氧化钠 |
| B |
明矾能水解生成Al(OH)3胶体 |
实验室用明矾与水反应制Al(OH)3 |
| C |
SiO2是酸性氧化物 |
SiO2与任何酸均不反应 |
| D |
Zn具有还原性和导电性 |
可用作锌锰干电池的负极材料 |
在中学化学实验中可用来分离或提纯物质的方法很多,如蒸馏、过滤、结晶、渗析、盐析等,分离或提纯下列各组混合物所选用方法最合适的是( )
| A.FeCl3溶液得到FeCl3固体——加热蒸干 |
| B.除去Cu粉中混有的CuO——加入稀硝酸溶解、过滤、洗涤、干燥 |
| C.分离NaNO3和BaSO4的混合物——溶解、过滤 |
| D.除去NaOH溶液中混有的少量Na2SO4——加入BaCl2溶液、过滤 |
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A.0.1 mol·L-1 NaOH溶液:K+、Ba2+、Cl-、HCO3- |
| B.0.1 mol·L-1 Na2CO3溶液:K+、NH4+、NO3-、SO42- |
| C.0.1 mol·L-1 FeCl3溶液:K+、Na+、I-、SCN- |
| D.0.1 mol·L-1 HCl的溶液:Ca2+、Na+、ClO-、NO3- |