要证明硬脂酸具有酸性,可采用的正确实验是()
| A.使硬脂酸溶于汽油,向溶液中加入石蕊试液,溶液变红 |
| B.把纯碱加入硬脂酸并微热,产生泡沫 |
| C.把硬脂酸加热熔化,加入金属钠,产生气泡 |
| D.向滴有酚酞的NaOH(aq)里加入硬脂酸,微热,红色变浅甚至消失 |
有Na2CO3、AgNO3、BaCl2 、HCl及NH4NO3五瓶无标签的溶液,为鉴别它们,取四支试管分别装入一种溶液,再向上边四支试管中加入少许剩下的一种溶液,则下列表述错误的是()
| A.若三支试管出现沉淀时,则后加入的是AgNO3 |
| B.全部没有什么现象变化时,则后加入的是NH4NO3 |
| C.一支试管出现气体,另两支试管出现沉淀时,最后加入的盐酸 |
| D.若只有两支试管出现沉淀时,则后加入的是BaCl2溶液 |
将标准状况下的V LHCl(气)溶于1000g水中,得到的盐酸密度为rg/cm3,则该盐酸的物质的量浓度为()
A.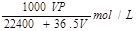 |
B. |
C. |
D.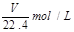 |
某氯原子的质量为a g,12C原子的质量为b g,用NA表示阿伏加德罗常数的值,下列说法中不正确的是()
| A.y g该氯原子所含的电子数为17y/a |
| B.x g该氯原子的物质的量一定是x/(a × NA)mol |
| C.1mol该氯原子的质量是aNA g |
| D.该氯原子的摩尔质量为a g/mol |
在20℃时一刚性容器内部有一不漏气且可滑动的活塞将容器分隔成左、右室两室。左室充入N2,右室充入H2和O2,活塞正好停留离左端1/5处(如右图a)然后点燃引爆H2和O2混合器,活塞先左弹(设容器不漏气),恢复至原来温度,活塞恰好停在中间(如右图b),水蒸气的体积可忽略,则反应前H2和O2的体积比可能是( )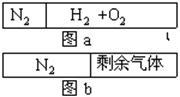
| A.1︰1 | B.1︰3 | C.7︰1 | D.5︰1 |
向一定量的饱和NaOH溶液中加入少量Na2O固体,恢复到原来温度时,下列说法中正确的是()
| A.溶液中的Na+总数不变 | B.溶液中的OH-数目不变 |
| C.溶质的物质的量浓度不变 | D.溶液的质量不变 |