| A.标准状况下,由5.6LNO和5.6LO2组成的混合气体中原子总数约为6.02 ×1023 |
| B.50mL0.1mol/LNaC1溶液中,微粒总数约为6.02 × 1021 |
| C.1mol甲基中电子总数约为6.02×1024 |
| D.22.4L乙炔中共用电子对总数约为1.806 ×1024 |
将5 mol O2在高温下放电,经过时间t后建立了3O2 2O3的平衡体系,已知O2的转化率为20%,下列浓度(c)变化曲线正确的是( )
2O3的平衡体系,已知O2的转化率为20%,下列浓度(c)变化曲线正确的是( )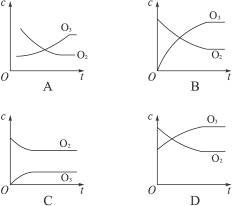
在5 L的密闭容器中充入2 mol A气体和1 mol B气体,在一定条件下发生如下反应:2A(g)+B(g) 2C(g)。达平衡时,在相同温度下测得混合气体的压强是反应前的
2C(g)。达平衡时,在相同温度下测得混合气体的压强是反应前的 ,则A的转化率为( )
,则A的转化率为( )
| A.67% | B.50% | C.2.5% | D.5% |
把6 mol A和5 mol B的混合气体通入容积为4 L的密闭容器中,在一定条件下发生如下反应:5A(g)+4B(g) 6C(g)+xD(g),经5 min后反应达到平衡,此时生成C 3 mol,并测得D的平均反应速率为0.1 mol·L-1·min-1。下列说法正确的是( )
6C(g)+xD(g),经5 min后反应达到平衡,此时生成C 3 mol,并测得D的平均反应速率为0.1 mol·L-1·min-1。下列说法正确的是( )
| A.x=2 |
| B.A的转化率是41.67% |
| C.B的平衡浓度为0.75 mol·L-1 |
D.反应前后混合气体的压强比为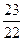 |
在t ℃时,向一密闭容器中放入1 mol A和1 mol B,发生下列反应:A(g)+B(g) C(g)+2D(g),平衡时C的含量为m%。其他条件不变,按下列配比将物质放入容器中,达平衡时,C的含量仍为m%的是( )
C(g)+2D(g),平衡时C的含量为m%。其他条件不变,按下列配比将物质放入容器中,达平衡时,C的含量仍为m%的是( )
A.2 mol A和1 mol B
B.2 mol D和A、B、C、各1 mol
C.1 mol C和2 mol D
D.1 mol C和1 mol D
已知常温常压和催化剂条件下,N2(g)和H2(g)生成2 mol NH3(g)放出92.4 kJ的热量。在上述条件下向密闭容器中通入1 mol N2和3 mol H2,达到平衡时放出热量为Q1 kJ;向另一体积相同的容器中通入0.9 mol N2、2.7 mol H2和0.2 mol NH3,相同条件下达到平衡时放出热量为Q2 kJ。则下列关系式正确的是( )
| A.2Q=Q1="92.4" | B.Q2<Q1<92.4 |
| C.Q1<Q2<92.4 | D.Q1=Q2=92.4 |