已知Fe有三种常见的氧化物FeO,Fe2O3,Fe3O4,其中Fe3O4可看成是FeO·Fe2O3,而铁的常见价态有+2和+3价,Fe2+遇到稀硝酸则发生氧化还原反应生成Fe3+和NO。写出上面三种氧化物和稀硝酸反应的方程式。
将几滴KSCN(SCN-是“类卤离子”)溶液加入到含有Fe3+的酸性溶液中,溶液变成红色。将该红色溶液分为两份:①一份中加入适量KMnO4溶液,红色褪去;②向另一份中通入SO2,红色也褪去。以下推测肯定不正确的是()
| A.①中红色褪去的原因是KMnO4将SCN-氧化 |
| B.②中红色褪去的原因是SO2将Fe3+还原成Fe2+ |
| C.②中红色褪去的原因是SO2将SCN-还原 |
| D.SCN-在适当条件下可失去电子被氧化为(SCN)2 |
将CO2气体缓缓地通入到含KOH、Ba(OH)2和KAlO2的混合溶液中直至过量,生成沉淀的物质的量与所通CO2的体积关系如图所示。下列关于整个反应进程中的各种描述不正确的是()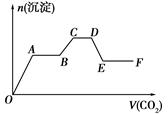
| A.O~A段反应的化学方程式是Ba(OH)2+CO2=BaCO3↓+H2O |
| B.B~C段反应的离子方程式是2AlO2-+3H2O+CO2=2Al(OH)3↓+CO32- |
| C.A~B段与C~D段所发生的反应相同 |
| D.D~E段沉淀的减少是由于碳酸钡固体的消失所致 |
下列装置、操作及说法正确的是()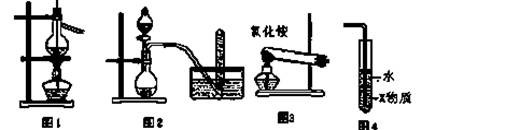
| A.图1用于海水蒸馏 | B.图2用于铜与浓硝酸反应制取NO2 |
| C.图3用于实验室制氨 | D.图4中X若为四氯化碳,可用于吸收氯化氢气体,并防止倒吸 |
设NA为阿伏加德罗常数的数值,下列说法中正确的是()
| A.标准状况下,22.4L Cl2完全溶于水时,转移电子数为NA |
| B.常温下, pH=l的H2SO4溶液中含有的H+的数目为0.2NA |
| C.标准状况下,2.24 L NH3中含有共价键的数目为NA |
| D.常温下,23 g NO2和N2O4的混合气体中含有NA个氧原子 |
元素周期表中铋元素的数据见图,下列说法正确的是()
| A.Bi元素的质量数是209 |
| B.Bi元素的相对原子质量是209.0 |
| C.Bi原子6p亚层(能级)有一个未成对电子 |
| D.Bi原子最外层有5个能量相同的电子 |