下列有水参加的氧化还原反应中,水既不是氧化剂,也不是还原剂的反应是( )
| A.2Na+2H2O====2NaOH+H2↑ |
| B.2F2+2H2O====4HF+O2 |
| C.3NO2+H2O====NO+2HNO3 |
| D.CO2+H2O====H2CO3 |
现有①NaOH②Al2(SO4)3③Ba(NO3)2 ④CuSO4 ⑤FeCl3⑥淀粉溶液⑦KI 这7种溶液
| A.不需外加试剂即可鉴别 | B.必须外加试剂才能鉴别 |
| C.如有碘水即能全部鉴别 | D.另有一种溶液即可鉴别 |
下列离子方程式中正确的是
| A.将SO2气体通入NaClO溶液中:SO2+2ClO-+H2O====SO32—+2HClO |
| B.FeI2溶液中通入少量Cl2:2Fe2++Cl2=2Fe3++2Cl- |
| C.在硫酸氢钾溶液中加入Ba(OH)2溶液至pH=7 2H++SO42-+Ba2++2OH-==BaSO4↓+2H2O |
| D.NH4HCO3溶液与少量NaOH溶液反应:NH++OH-=NH3·H2O |
将F2通入到热的NaOH溶液中可发生氧化还原反应,其中F2和NaOH等物质量进行反应,生成物中有NaF、H2O和另一种气体,则该气体可能是
| A.H2 | B.HF | C.OF2 | D.O2 |
下列关于氨气的说法正确的是
| A.氨气可以用碱石灰干燥也可用无水CaCl2干燥 |
| B.氨水能导电,所以NH3是电解质 |
| C.沸点:NH3<PH3<AsH3 |
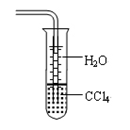
| D.用水吸收NH3用下图装置可防止倒吸: |
室温下,下列各组离子在指定溶液中一定能大量共存的是
A.饱和氯水中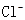 、 、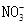 、 、 、 、 |
B.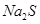 溶液中 溶液中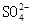 、 、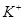 、 、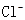 、 、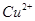 |
C.pH=13的溶液中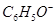 、 、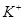 、 、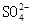 、 、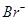 |
D.由水电离 溶液中 溶液中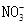 、 、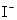 、 、 、 、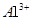 |