25 ℃时,在0.1 mol·L-1 C(H+)=1.32×10-3 mol·L-1的CH3COOH溶液中,水的离子积是( )
| A.1×10-14 | B.1×10-13 | C.1.32×10-14 | D.1.32×10-5 |
下列有关平衡常数的说法正确的是
A.已知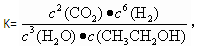 则对应的化学反应可以表示为: 则对应的化学反应可以表示为:2CO2(g) + 6H2(g) 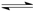 CH3CH2OH(g) + 3H2O(g) CH3CH2OH(g) + 3H2O(g) |
| B.将某浓度醋酸溶液升高温度,醋酸的电离平衡常数Ka将变大 |
| C.常温下,向纯水中加入少量碳酸钠固体,水的电离程度变大,Kw变大 |
D.常温下,在饱和氯水中加入少量碳酸钙固体,Cl2+H2O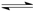 HCl+HClO平衡正移,平衡常数K变大 HCl+HClO平衡正移,平衡常数K变大 |
在容积不变的密闭容器中进行反应:2SO2(g)+O2(g) 2 SO3(g)△H<0。下列各图表示当其他条件不变时,改变某一条件对上述反应的影响,其中分析正确的是
2 SO3(g)△H<0。下列各图表示当其他条件不变时,改变某一条件对上述反应的影响,其中分析正确的是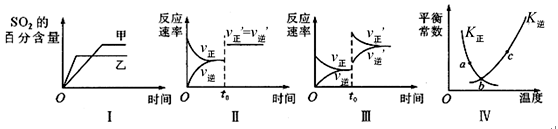
| A.图I表示温度对化学平衡的影响,且甲的温度较高 |
| B.图Ⅱ表示t0时刻使用催化剂对反应速率的影响 |
| C.图Ⅲ表示t0时刻增大O2的浓度对反应速率的影响 |
| D.图Ⅳ中a、b、c三点中只有b点已经达到化学平衡状态 |
下列各组离子在酸性溶液中能大量共存的是
| A.K+、ClO-、Ba2+、HCO3- |
| B.Na+、Al3+、NO3-、SO42- |
| C.Fe3+、K+、SCN-、Cl- |
| D.Mg2+、NH4+、Fe2+、NO3- |
把石墨棒和铁片用下列a、b两种方式放在盛有稀食盐水和酚酞试液混合溶液的玻璃器皿中,经过一段时间后,首先观察到溶液变红的区域是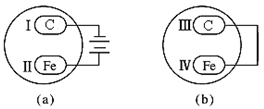
| A.Ⅰ和Ⅲ附近 | B.Ⅰ和Ⅳ附近 | C.Ⅱ和Ⅲ附近 | D.Ⅱ和Ⅳ附近 |
下列关于CO2与SO2说法不正确的是
| A.都是无色气体 | B.都是非电解质 |
| C.通入Ba(OH)2溶液中都能产生白色沉淀 | D.都是形成酸雨的主要原因 |