一个密闭容器,中间有一可自由滑动的隔板(厚度或忽略)将容器分成两部分,当左边充入1molN2,右边充入CO和CO2的混合气体共9g时,隔板处于如图位置(左、右两侧温度相同),求混合气体中CO和CO2的分子个数比。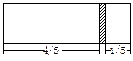
向1L AlCl3和FeCl3混合溶液中加入含a mol NaOH的溶液时,产生的沉淀量可达最大值;继续加入NaOH溶液,沉淀开始溶解,当前后加入的NaOH总量达到b mol时,沉淀不再减少,求原溶液中Fe3+的物质的量浓度。
(10分)在10mL含有AlO2-离子的溶液中逐滴加入1mol/L的盐酸,所得Al(OH)3沉淀质量和所加盐酸的体积关系如图所示。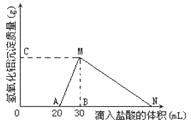
问:(1)此溶液中除含有AlO2- 外,还同时含有____mol___离子;
(2)用离子方程式表示MN段发生的反应是
(3)原溶液中,c (AlO2-) 是 mol/L
(4)加盐酸到点N处,滴入的HCl溶液体积共为ml
按右图的装置进行电解实验:A极是铜锌合金,B极为纯铜,电解质中含有足量的铜离子。通电一段时间后,若A极恰好全部溶解,此时B极质量增加7.68克,溶液质量增加0.03克,则A合金中Cu、Zn原子个数比为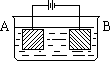
| A. 4︰1 | B.3︰1 | C. 2︰1 | D.任意比 |
用KMnO4氧化密度为1.19g/cm3,溶质质量为36.5%的 HCl.反应方程式如下:2KMnO4 + 16HCl = 2KCl + 2MnCl 2+ 5Cl 2↑+ 8H2O
(1)15.8g KMnO4能使多少克HCl发生上述反应?有多少克HCl被氧化?
(2)若Cl 2在标准状况下的密度为3.17g/L,则产生的Cl 2在标准状况下的体积为多少?
用MnO2,和浓HCl反应制Cl2,当有0.4molHCl被氧化时,生成的Cl2全部用石灰水吸收,则(1)生成多少Cl2mol(2)可制得漂白粉多少克?