取50.0 mL Na2CO3和Na2SO4的混合溶液,加入过量BaCl2溶液后得到14.51 g白色沉淀,用过量稀硝酸处理后沉淀质量减少到4.66 g,并有气体放出。试计算:
(1)原混合溶液中Na2SO4和Na2CO3的物质的量浓度。
(2)产生的气体在标准状况下的体积。
向500ml盐酸中投入11.2克铁,二者恰好完全反应(忽略体积变化),计算:
(1)反应后所得溶液的物质的量浓度
(2)生成标准状况下H2的体积。
火箭的主要燃料是“偏二甲肼”,已知该化合物由C.H、N三种元素组成, WC=40%,WH=13.33%,其分子量为60。通过结构分析可知,该物质分子中其中有一个氮原子以 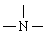 存在,且不与H原子直接相连。燃料的氧化剂是N2O4,燃烧产物只有CO2、H2O、N2;5.00g“偏二甲肼”完全燃烧时可放出212.5kJ热量。
存在,且不与H原子直接相连。燃料的氧化剂是N2O4,燃烧产物只有CO2、H2O、N2;5.00g“偏二甲肼”完全燃烧时可放出212.5kJ热量。
(1)试推算“偏二甲肼”的分子式,并写出它的结构简式。
(2)写出燃料燃烧的热化学方程式。
一定温度下,密闭容器中M、N、R三种气体的初始浓度和平衡浓度如下表所示:
| 物质 |
M |
N |
R |
| 初始浓度/mol•L—1 |
0.20 |
0.30 |
0 |
| 平衡浓度/mol•L—1 |
0.02 |
0.21 |
0.18 |
(1)请通过计算写出此反应的化学方程式。
(2)达平衡时,N的转化率是多少?
按下图装置进行实验,并回答下列问题
(1)判断装置的名称:B池为
(2)铜极为______极,电极反应式为
石墨棒C2附近发生的实验现象为
(3)当C2极析出224mL气体(标准状态时,锌的质量变化(增加或减少)g.
CuSO4溶液的质量变化了(增加或减少了)g .
某混合气体由一种气态烷烃和一种气态烯烃组成,在同温同压下,混合气体对氢气的相对密度为13,在标准状况下,将56.0L混合气体通入足量溴水,溴水质量增重35.0g,通过计算回答:
(1)混合气体中气态烷烃的化学式
(2)混合气体中两种气体的物质的量之比
(3)写出混合气体中气态烯烃可能的结构简式(包括顺反异构体)