有碳原子数相同的烯烃、炔烃混合气aL,完全燃烧后生成bL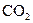 和cL水蒸气
和cL水蒸气
(温度、压强与原混合气相同),若a∶b∶c=3∶6∶4,则下列叙述中正确的是
| A.原混合气为体积比是1∶1的丙烯和丙炔 |
| B.原混合气为任意体积比的乙烯和乙炔 |
| C.原混合气为体积比为2∶1的丁烯和丁炔 |
| D.原混合气为体积比为1∶2的乙烯和乙炔 |
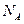 表示阿伏加德罗常数,下列说法正确的是()
表示阿伏加德罗常数,下列说法正确的是()
A.氟气与水反应生成1moL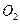 共转移 共转移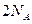 个电子 个电子 |
B.标准状况下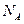 个 个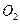 分子的质量与 分子的质量与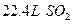 气体的质量大致相等 气体的质量大致相等 |
C.含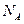 个负电荷的 个负电荷的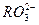 离子的质量为40g 离子的质量为40g ,则 ,则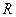 的摩尔质量为32g·mol–1 的摩尔质量为32g·mol–1 |
D.25℃时,pH=13的烧碱溶液中约含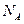 个氢氧根( 个氢氧根(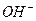 )离子 )离子 |
H2O2可以作为脱氯剂,反应方程式为:H2O2+Cl2==2HCl+O2,下列说法错误的是()
| A.该反应为置换反应 | B.生成1mol O2需转移电子4mol |
| C.H2O2被氧化 | D.H2O2分子中含极性共价键 |
下列各项中,碱金属元素随原子序数的增加,跟卤族元素变化不一致的是()
| A.单质的熔沸点 | B.原子半径 |
| C.单质的密度 | D.原 子的电子层数 子的电子层数 |
普通锌锰干电池的简图(如右下图所示),它是用锌皮制成的锌筒作电极兼做容器,中央插一根碳棒,碳棒顶端加一铜帽。在石墨碳棒周围填满二氧化锰和炭黑的混合物,并用离子可以通过的长纤维纸包裹作隔膜,隔膜外是用氯化锌、氯化铵和淀粉等调成糊状作电解质溶液;该电池工作时的总反应为:
Zn+2NH4++2MnO2=[Zn(NH3)2]2++Mn2O3+H2O
关于锌锰干电池的下列说法中正确的是( ▲ ) 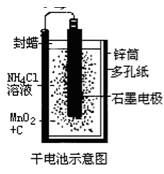
| A.当该电池电压逐渐下降后,利用电解原理能重新充电复原 |
| B.电池正极的电极反应式为: 2MnO2+2NH4++2e- ="=" Mn2O3+2NH3+H2O |
| C.电池工作时,电子由正极通过外电路流向负极 |
| D.外电路中每通过0.1 mol电子,锌的质量理论上减小6.5g |
将炭粉和铁粉均匀混合,撒入内壁分别用氯化钠溶液和稀醋酸溶液润湿过的具支试管中,并按下图装置好仪器,观察下图,示意正确的是( ▲ )