下列关于实验或说法正确的是( )
| A.SO2能使品红溶液、酸性KMnO4溶液褪色,加热后都能复原 |
| B.用铂丝蘸取某溶液在酒精灯火焰上灼烧,透过蓝色钴玻璃观察到火焰颜色为紫色,说明原溶液中不含Na+ |
| C.用滴加BaCl2溶液,观察有无白色沉淀的方法来鉴别K2CO3和NaHCO3 |
| D.少量CO2通过CaCl2的溶液能生成白色沉淀,过量CO2时白色沉淀溶解 |
在一定温度下,一定量的水中,石灰乳悬浊液存在下列平衡:Ca(OH)2(s) 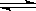 Ca(OH)2(aq)
Ca(OH)2(aq) 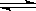 Ca2+(aq) + 20H-(aq),当向此悬浊液中加入少量氢氧化钙时,下列说法正确的是( )
Ca2+(aq) + 20H-(aq),当向此悬浊液中加入少量氢氧化钙时,下列说法正确的是( )
| A.[Ca2+]增大 | B.[Ca2+]不变 | C.[OH-]增大 | D.[OH-]不变 |
下列物质的溶解度随温度升高而减小的是( )
| A.KN03 | B.Ca(OH)2 | C.BaS04 | D.CO2 |
列属于微溶物质的是( )
| A.AgCl | B.BaCl2 | C.CaSO4 | D.Ag2S |
某温度下向100g澄清的饱和石灰水中加入5.6g生石灰,充分反应后恢复到原来的温度。下列叙述正确的是()
| A.沉淀物的质量为5.6g | B.沉淀物的质量为7.4g |
| C.饱和石灰水的质量大于98.2g | D.饱和石灰水的质量小于98.2g |
S02通人BaCl2溶液至饱和未见沉淀,继续通入另一气体仍无沉淀。则通入的气体可能是 ( )
| A.CO2 | B.NH3 | C.NO2 | D.H2S |