一带有活塞的密封容器中盛有A、B组成的混合气体,在通常条件下,从状态I反应到状态II时,气体体积(V)与气体压强(P)的变化曲线如图所示。 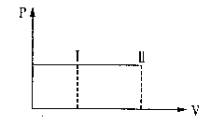
则反应:A(g)+B(g)="2C(g)"
A.是放热反应 B.反应后气体总分子数增多
C.是吸热反应 D.反应物具有的总能量等于生成物具有的总能量
用来表示可逆反应:2A(g)+B(g) 2C(g)ΔH<0的正确图象是下图中的()
2C(g)ΔH<0的正确图象是下图中的()
A B C D
有一可逆反应 2A(g)+3B(g) xC(g),若按下列两种配比在同温同容积的密闭容器中进行反应:
xC(g),若按下列两种配比在同温同容积的密闭容器中进行反应:
⑴0.8 mol A、1.2 mol B、1.2 mol C ⑵1.4 mol A、2.1 mol B、0.6 mol C
达到平衡后,C的百分含量相等,则该化学方程式中x的值可能为
A.2 B.3C.4 D.5
下列事实不能用勒夏特列原理解释的是
A.溴水中有平衡:Br2+H2O HBr+HBrO,当加入AgNO3溶液后,溶液颜色变浅。 HBr+HBrO,当加入AgNO3溶液后,溶液颜色变浅。 |
B.对CO(g)+NO2(g) CO2(g)+NO(g),平衡体系增大压强可使颜色变深。 CO2(g)+NO(g),平衡体系增大压强可使颜色变深。 |
| C.升高温度能够促进水的电离。 |
| D.工业上合成NH3的反应,为提高NH3的产率,理论上应采取相对较低温度的措施。 |
醋酸溶液中存在电离平衡: 下列叙述不正确的是
下列叙述不正确的是
A.CH3COOH溶液中离子浓度的关系满足: |
B.0.1 mol / L 的CH3COOH 溶液加水稀释,溶液中c( )减小 )减小 |
| C.CH3COOH溶液中加入少量CH3COONa固体,平衡逆向移动 |
| D.常温下,pH=2的CH3COOH溶液与pH=12的NaOH 溶液等体积混合后,溶液 |
的pH<7
工业上制备纯硅反应的热化学方程式如下:
SiCl4(g)+2H2(g) =" Si(s)+4HCl(g)"  mol(Q>0)
mol(Q>0)
某温度、压强下,将一定量反应物通入密闭容器进行以上反应(此条件下为可逆反应),下列叙述正确的是
| A.反应过程中,若增大压强能提高SiCl4的转化率 |
| B.若反应开始时SiCl4为1 mol,则达平衡时,吸收热量为Q kJ |
| C.反应至4 min时,若HCl浓度为0.12 mol/L,则H2的反应速率为0.03 mol/(L·min) |
| D.当反应吸收热量为0.025Q kJ时,生成的HCl通入100 mL 1 mol/L的NaOH溶液恰好反应 |