在下列四种溶液中,分别加入少量固体二氧化锰,能产生气体的是( )
| A.3% H2O2溶液 |
| B.1 mol·L-1 NaOH 溶液 |
| C.1 mol·L-1 KClO3溶液 |
| D.1 mol·L-1盐酸 |
哈伯因发明了由氮气和氢气合成氨气的方法而获1918年诺贝尔化学奖。现向一密闭容器中充入1mol N2和3mol H2,在一定条件下使该反应发生。下列有关说法正确的是()
| A.达到化学平衡时,N2将完全转化为NH3 |
| B.达到化学平衡时,N2、H2和NH3的物质的量浓度一定相等 |
| C.达到化学平衡时,N2、H2和NH3的物质的量浓度不再变化 |
| D.达到化学平衡时,正反应和逆反应的速率都为零 |
化学反应A2+B2===2AB的能量变化如图所示,则下列说法正确的是( )
| A.该反应是吸热反应 |
| B.断裂1 mol A—A 键和1 mol B—B 键放出x kJ能量 |
| C.断裂2 mol A—B 键需要吸收y kJ的能量 |
| D.2 mol AB的总能量高于1 mol A2和1 mol B2的总能量 |
下列说法正确的是( )
| A.含有共价键的化合物必是共价化合物 |
| B.阴、阳离子间通过静电引力所形成的化学键是离子键 |
| C.化学变化过程,一定会破坏旧的化学键,同时形成新的化学键 |
| D.液态氯化氢中存在H+和Cl-,所以能导电 |
下列各组性质比较中,正确的是( )
①酸性:HClO4>HBrO4>HIO4②碱性:Ba(OH)2>Mg(OH)2>Be(OH)2
③氧化性:F>C>O④氧化性:Li+﹤Na+﹤K+
⑤气态氢化物稳定性:HF>HCl>H2S
| A.①②③ | B.②③④ | C.①②⑤ | D.①②④⑤ |
下列各组物质中互为同位素的是( )
A.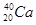 和 和 |
B.D和T |
C.H2O和H2O2 | D.O3和O2 |