将2 mol A和2 mol B充入某密闭容器中发生反应:2A(g)+B(g) xC(g),达到化学平衡后,C的体积分数为a。假设该反应的条件分别和下列各选项的条件相同,下列判断正确的是( )
xC(g),达到化学平衡后,C的体积分数为a。假设该反应的条件分别和下列各选项的条件相同,下列判断正确的是( )
A.若在恒温恒容下,当x=1时,将1 mol B\,1 mol C作为起始物质,达到平衡后,C的体积分数不是a
B.若在恒温恒容下,当x=2时,将2 mol C作为起始物质,达到平衡后,C的体积分数大于a
C.若在恒温恒容下,当x=3时,将2 mol B、6 mol C作为起始物质,达到平衡后,C的体积分数不等于a
D.若在恒温恒压下,将3 mol A\,3 mol B作为起始物质,达到平衡后,C的体积分数仍为a,则x可为任意正整数
要检验某溴乙烷中的溴元素,正确的实验方法是( )
| A.加入溴水振荡,观察水层是否有棕红色出现 |
| B.滴入AgNO3溶液,再加入稀硝酸呈酸性,观察有无浅黄色沉淀生成 |
| C.加入NaOH溶液共热,然后加入稀硝酸呈酸性,再滴入AgNO3溶液,观察有无浅黄色沉淀生成 |
| D.加入NaOH溶液共热,冷却后滴入AgNO3溶液,观察有无浅黄色沉淀生成 |
有机物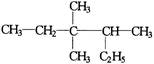 的正确命名为()
的正确命名为()
| A.2-乙基-3,3-二甲基-4-乙基戊烷 | B.3,3-二甲基-4-乙基戊烷 |
| C.3,3,4-三甲基已烷 | D.2,3,3-三甲基已烷 |
写出下列元素原子的电子排布式
P,Cr,
Al,Cu,
下列叙述中正确的是( )
A.BF3、H2O和NH3都是极性分子
B CO2和 C2H4都是含有极性键的非极性分子
C.HF、HCl、HBr、HI稳定性依次增强
D.NH3、SiH4、SO3都是四面体型分子
主族元素X和Y ,Xm-和Yn+核外电子排布相同,下列说法正确的为( )
| A.X的原子半径大于Y | B.X和Y的核电荷数之差为m-n |
| C.电负性X>Y | D.第一电离能X<Y |