在t ℃时,向一密闭容器中放入1 mol A和1 mol B,发生下列反应:A(g)+B(g) C(g)+2D(g),平衡时C的含量为m%。其他条件不变,按下列配比将物质放入容器中,达平衡时,C的含量仍为m%的是( )
C(g)+2D(g),平衡时C的含量为m%。其他条件不变,按下列配比将物质放入容器中,达平衡时,C的含量仍为m%的是( )
A.2 mol A和1 mol B
B.2 mol D和A、B、C、各1 mol
C.1 mol C和2 mol D
D.1 mol C和1 mol D
下列能用勒夏特列原理解释的是
①棕红色NO2加压后颜色先变深后变浅②FeCl3溶液加热后颜色加深
③Fe(SCN)3溶液中加入固体KSCN后颜色变深④氯水宜保存在低温、避光条件下⑤向H2S水溶液中加入NaOH有利于S2-增多⑥合成氨时将氨液化分离,可提高原料的利用率⑦向AgCl悬浊液中加入KI溶液有黄色沉淀生成
| A.①②⑤⑥ | B.②③④⑦. | C.①③⑤⑦ | D.全部 |
1,2,3-三苯基环丙烷的三个苯基可以分布在环丙烷环平面的上下,从而形成异构体,如右图所示。据此可知1,2,3,4,5五氯环戊烷(假定其五个碳原子在同一平面上)的异构体数目是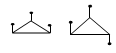
| A.4 | B.5 | C.6 | D.7 |
在水中加入等物质的量的Ag+、Pb2+、Na+、SO42-、NO3-、Cl-,用惰性电极电解此溶液,通电片刻,则氧化产物与还原产物的质量比为
| A.35.5:10.8 | B.16:207 | C.8:1 | D.108:35.5 |
利用下列实验装置及药品(依次为①—④)能完成相应实验的是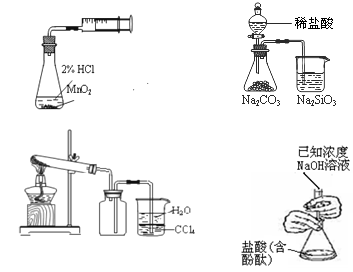
| A.实验①测定化学反应速率 | B.②能证明非金属性 Cl>C>Si |
| C.实验③制取并收集NH3 | D.滴定法测定盐酸浓度 |
高功率Ni/MH(M表示储氢合金)电池已经用于混合动力汽车。总反应方程式如下:
下列叙述不正确的是
| A.该电池放电时的正极和充电时的阴极均发生还原反应 |
| B.放电时负极反应为:MH+OH——e— = M+H2O |
| C.充电时阳极反应为:NiOOH+H2O+e— = Ni(OH)2+OH— |
| D.放电时每转移1mol电子,正极有1molNiOOH被还原 |