德国和美国科学家首次制造出了由20个碳原子组成的空心笼状分子C20,该笼状结构是由许多正五边形构成的(如图所示),下列有关C20的说法不正确的是( )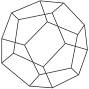
| A.C20与C60、C70互为同素异形体 | B.C20中有12个五边形,30条棱边 |
| C.C20具有很高的硬度和熔沸点 | D.C20的摩尔质量是240 g·mol-1 |
硫酸钡不容易被X射线透过,在医疗上可作检查肠胃的内服药剂。硫酸钡属于
| A.酸 | B.混合物 | C.氧化物 | D.盐 |
下列仪器中,不能用来加热的是
| A.容量瓶 | B.蒸发皿 | C.蒸馏烧瓶 | D.试管 |
进行淀粉水解实验(包括检验水解产物及水解是否完全)时,除淀粉外,还使用下列试剂(或试纸):
(1)碘水;(2)银氨溶液;(3)NaOH溶液;(4)稀硫酸;(5)pH试纸。
使用上述试剂的顺序依次是
| A.(4)(1)(3)(5)(2) | B.(4)(1)(2)(3)(5) |
| C.(1)(2)(3)(4)(5) | D.(4)(1)(3)(2)(5) |
欲将蛋白质从水中析出而又不改变它的性质应加入
| A.甲醛溶液 | B.饱和Na2SO4溶液 | C.CuSO4溶液 | D.浓硫酸 |
下列物质不能为动物体提供能量的是
| A.脂肪 | B.蛋白质 | C.糖类 | D.微量元素 |