随着人们生活质量的不断提高,废电池必须进行集中处理的问题被提到议事日程上来,其首要原因是( )
| A.利用电池外壳的金属材料 |
| B.防止电池中汞、镉和铅等重金属离子对土壤和水源的污染 |
| C.不使电池中渗泄的电解液腐蚀其他物品 |
| D.回收其中石墨电极 |
在容积不变的密闭容器中进行反应:2SO2(g)+O2(g) 2 SO3(g) △H<0。下列各图表示当其他条件不变时,改变某一条件对上述反应的影响,其中分析正确的是
2 SO3(g) △H<0。下列各图表示当其他条件不变时,改变某一条件对上述反应的影响,其中分析正确的是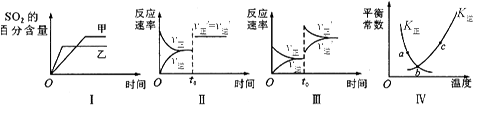
| A.图I表示温度对化学平衡的影响,且甲的温度较高 |
| B.图Ⅱ表示t0时刻使用催化剂对反应速率的影响 |
| C.图Ⅲ表示t0时刻增大O2的浓度对反应速率的影响 |
| D.图Ⅳ中a、b、c三点中只有b点已经达到化学平衡状态 |
对于反应CO2(g)+H2(g)  CO(g)+H2O(g) ΔH>0,在其他条件不变的情况下
CO(g)+H2O(g) ΔH>0,在其他条件不变的情况下
| A.加入催化剂,改变了反应的速率,反应的ΔH也随之改变 |
| B.降低温度,反应速率减慢,反应放出的热量不变 |
| C.改变反应体系体积,平衡不发生移动,反应放出的热量不变 |
| D.若将上述反应改为在燃料电池进行,反应放出的热量不变 |
室温下,强酸性和强碱性溶液中都不能共存的离子组是
| A.NH4+、Cu2+、SO42-、NO3- | B.K+、Na+、SO32-、S2- |
| C.K+、Na+、Al3+、SO42- | D.Mg2+、Fe2+、NO3-、I- |
下列说法中,正确的是
| A.Na2O和Na2O2组成元素相同,且都能与硫酸溶液反应 |
| B.光导纤维由SiO2制备得到,其属于硅酸盐产品 |
| C.工业上利用电解熔融的MgO来制备镁 |
| D.SO2通入新制氯水中,氯水褪色是因为SO2具有漂白性 |
分类是科学研究的重要方法,下列物质分类不正确的是
| A.非电解质:乙醇,氯气,葡萄糖 |
| B.化合物:冰水混合物,烧碱,小苏打 |
| C.分子晶体:干冰,碘单质,蔗糖 |
| D.混合物:铝热剂,纯净矿泉水,分析纯盐酸 |