阿伏加德罗常数(NA)、物质的量(n)和粒子数(N)之间有如下关系:NA=N/n,测定阿伏加德罗常数有多种方法,其中电解法是常用的方法。实验室有同样浓度的KCl、CuCl2、AgNO3、H2SO4等溶液,若实验过程中不考虑电极上的析出物与电解后的溶液之间的反应,则你认为选用哪一种溶液作为电解液,实验既简便、测定结果误差又小。
| A.KCl | B.CuCl2 | C.AgNO3 | D.H2SO4 |
下列说法中正确的是
| A.卤代烃在NaOH存在下水解生成的有机物都是醇 |
| B.所有的一元醇都能被氧化为具有相同碳原子数的醛或酮 |
C.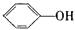 与 与 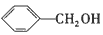 互为同系物 互为同系物 |
| D.分子式为C3H8与C6H14的两种有机物一定互为同系物 |
下列关于铁的叙述正确的是
①铁能被磁铁吸引,但纯铁易被腐蚀
②在人体内的血红蛋白中含有铁元素
③铁位于元素周期表中第四周期第ⅧB族
④铁能在氧气中剧烈燃烧,但不能在水蒸气中燃烧
⑤铁与强氧化剂硝酸反应的产物仅有Fe(NO3)3
⑥不能通过化合反应制得FeCl2和Fe(OH)3.
| A.①③ | B.②④ | C.②⑤ | D.④⑥ |
分子式为C8H16O2的有机物A,它能在酸性条件下水解生成B和C,且B在一定条件下能转化成C。则有机物A的可能结构有
A.1种B.2种C.4种D.8种
分子式为C5H10O3的有机物与NaHCO3溶液反应时,生成C5H9O3Na;而与金属钠反应时生成C5H8O3Na2。则该有机物的同分异构体的种类(不考虑立体异构)有
| A.10种 | B.11种 | C.12种 | D.13种 |
氯化硼的熔点为-107℃,沸点为12.5℃,在其分子中键与键之间的夹角为120°,它能水解,有关叙述正确的是
| A.氯化硼液态时能导电而固态时不导电 | B.硼原子以sp杂化 |
| C.氯化硼遇水蒸气会产生白雾 | D.氯化硼分子属极性分子 |