吸入人体内的O2有2%转化为氧化性极强的活性氧副产物,如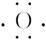 等,这些活性氧能加速人体衰老,被称为“夺命杀手”。我国科学家尝试用含硒化合物Na2SeO3来消除人体内的活性氧,在消除活性氧时,Na2SeO3的作用是( )
等,这些活性氧能加速人体衰老,被称为“夺命杀手”。我国科学家尝试用含硒化合物Na2SeO3来消除人体内的活性氧,在消除活性氧时,Na2SeO3的作用是( )
| A.还原剂 | B.氧化剂 | C.既是氧化剂,又是还原剂 | D.以上均不是 |
将22.4 g铁粉逐渐加入到含HNO3 0.8 mol的稀硝酸中,反应生成的气体的物质的量(x)随消耗铁粉的物质的量(y)变化关系中正确的是( )
如图,在注射器中加入少量Na2SO3晶体,并吸入少量浓硫酸(以不接触纸条为准)。则下列有关说法正确的是( )
| A.蓝色石蕊试纸先变红后褪色 |
| B.品红试纸、沾有KMnO4溶液的滤纸均褪色证明了SO2具有漂白性 |
| C.湿润淀粉KI试纸变蓝 |
| D.NaOH溶液可用于除去实验中多余的SO2 |
某短周期非金属元素的原子核外最外层电子数是次外层电子数的一半,该元素( )
| A.在自然界中只以化合态的形式存在 |
| B.单质常用作半导体材料和光导纤维 |
| C.最高价氧化物不与酸反应 |
| D.气态氢化物比甲烷稳定 |
下列实验现象与对应结论均正确的是()
| 选项 |
操作 |
现象 |
结论 |
| A |
常温下将Cu片放入浓H2SO4中 |
生成刺激性气味气体 |
Cu与浓H2SO4反应生成SO2 |
| B |
Al2(SO4)3溶液中滴加过量氢氧化钡溶液 |
生成白色沉淀 |
Al(OH)3不溶于氢氧化钡溶液 |
| C |
向某溶液中加入KSCN溶液,再向溶液中加入新制氯水 |
溶液先不显红色,加入氯水后变红色 |
该溶液中含有Fe2+ |
| D |
向某溶液中加入CCl4,振荡后静置 |
液体分层,下层呈紫红色 |
该溶液中存在I- |
相同pH等体积的氨水和NaOH溶液,各加入5mL 0.2mol·L-1AlCl3溶液。下列判断正确的是
| A.氨水中沉淀一定比NaOH溶液中的多 |
| B.氨水中沉淀一定比NaOH溶液中的少 |
| C.氨水中沉淀可能比NaOH溶液中的多 |
| D.氨水中和NaOH溶液中的沉淀不可能一样多 |