实验表明,不能用块状大理石与稀硫酸制取CO2气体,而能用大理石粉末与稀硫酸制取CO2气体。由此得出的合理结论是( )
| A.反应的物质之间是否发生反应,与反应的条件有关 |
| B.反应物之间接触面积越大,越有利于反应的进行 |
| C.块状大理石与大理石粉末的化学性质不同 |
| D.块状大理石与大理石粉末中各元素原子间电子的结合状况不同 |
几种短周期元素的原子半径及主要化合价如下表:
| 元素代号 |
X |
Y |
Z |
W |
| 原子半径/pm |
160 |
143 |
70 |
66 |
| 主要化合价 |
+2 |
+3 |
+5、+3、-3 |
-2 |
下列叙述正确的是
A.X、Y元素的金属性X<Y
B.一定条件下,W单质可以将Z单质从其氢化物中置换出来
C.Y的最高价氧化物对应的水化物能溶于稀氨水
D.一定条件下,Z单质与W的常见单质直接生成ZW2
下图是周期表中短周期的一部分.若X原子最外层电子数目比次外层电子数目少3个,则下列说法中不正确的是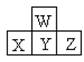
| A.X、Y、Z最高价氧化物对应水化物的酸性强弱关系是Z>Y>X |
| B.X的氢化物比Z的氢化物不稳定 |
| C.X、Y、Z各元素最高正价和最低负价的绝对值的和为8 |
| D.原子半径的大小顺序是Z>Y>X>W |
下列各组物质中化学键的类型相同的是
| A.HCl MgCl2 NH4Cl | B.H2O Na2O CO2 |
| C.CaCl2 NaOH H2O | D.NH3 H2O CO2 |
下表为元素周期表前4周期的一部分,且X、Y、Z、R和W为主族元素。下列说法正确的是
| X |
||
| Y |
Z |
R |
| W |
A.五种元素的原子最外层电子数一定大于2
B.五种元素一定都是非金属元素
C.Z的氧化物与X单质在任何条件下都不会发生置换反应
D.R的最外层电子数一定为5
W、X、Y、Z四种元素是原子序数依次增大的短周期主族元素,已知:①四种元素的电子层数之和等于10,且它们是连续的四种主族元素;②四种元素的原子,其半径最大的是X原子。下列说法正确的是
| A.W和X均位于第二周期 | B.Y和Z分别是Al和Si |
| C.W和X分别是O和F | D.Z的金属性可能比X强 |