为实现中国消除碘缺乏病的目标,卫生部规定食盐必须加碘,其中的碘以碘酸钾(KIO3)形式存在。已知在溶液中IO3-可和I-发生反应:IO3-+5I-+6H+=3I2+3H2O根据此反应,可用试纸和一些生活中常见的物质进行实验,证明在食盐中存在IO3-。可供选用的物质有:①自来水,②蓝色石蕊试纸,③碘化钾淀粉试纸,④淀粉,⑤食糖,⑥食醋,⑦白酒。进行上述实验时必须使用的物质是(碘单质可使淀粉变蓝色,用于碘的检验)
| A.①③ | B.③⑥ | C.②④⑥ | D.①②④⑤⑦ |
用NA表示阿伏加德罗常数的值,下列说法中正确的是( )
| A.标准状况下,22.4 L H2O含有NA个水分子 |
| B.标准状况下,22.4 L空气含有NA个单质分子 |
| C.常温常压下,11.2 L氯气所含的原子数目为NA |
| D.标准状况下,1.12 L O2和1.12 L CO2均含有0.1NA氧原子 |
实验室需配制一种仅含四种离子(不包括水电离出的离子)的混合溶液,且在混合液中四种离子的物质的量浓度均为0.5 mol·L-1,下面四个选项中能达到此目的的是( )
A.Fe2+、Na+、NO 、Cl- 、Cl- |
B.Mg2+、NH 、SO 、SO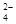 、NO 、NO |
| C.H+、K+、Cl-、CH3COO- | D.K+、Mg2+、CO 、OH- 、OH- |
有一种固体化合物M,M本身不导电,但熔融状态或溶于水均能够电离,下列关于M的说法中,正确的是( )
| A.M只能是碱类 | B.M只能是盐类 | C.M一定为电解质 | D.M可能为非电解质 |
下列与“物质的量”相关的计算正确的是( )
| A.5.6 g CO和22.4 L CO2中含有的碳原子数一定相等 |
B.n g Cl2中有m个Cl原子,则阿伏加德罗常数NA的数值可表示为 |
| C.标准状况下,11.2L M气体分子的质量为16 g,则M气体的摩尔质量是32 |
| D.现有CO、CO2、O3三种气体,它们均含有1 mol O,则三种气体的物质的量之比为3∶2∶1 |
使用容量瓶配制溶液时,由于操作不当,会引起误差,下列情况会使所配溶液浓度偏低的是( )
①用天平称量时,被称量物与砝码的位置放颠倒了
②溶液转移到容量瓶后,烧杯及玻璃棒未用蒸馏水洗涤
③定容时,俯视容量瓶的刻度线
④定容后摇匀,发现液面降低,又补加少量水,重新达到刻度线
| A.①②④ | B.①④ | C.③④ | D.②④ |