在标准状况下,向100 mL氢硫酸溶液中通入二氧化硫气体,溶液pH变化如图所示,则原氢硫酸溶液的物质的量浓度为( )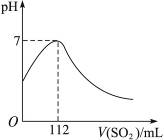
| A.0.5 mol·L-1 |
| B.0.05 mol·L-1 |
| C.1 mol·L-1 |
| D.0.1 mol·L-1 |
实验室欲用Na2CO3﹒10H2O晶体配制1mol/L的Na2CO3溶液100mL,下列说法正确的是
| A.要完成实验需称取10.6gNa2CO3﹒10H2O晶体 |
| B.本实验需用到的仪器是天平、药匙、玻璃棒、烧杯、100mL容量瓶 |
| C.配制时若容量瓶不干燥,含有少量蒸馏水会导致浓度偏低 |
| D.定容时俯视刻度线会导致浓度偏高 |
实现下列变化,一定要加入其它物质作氧化剂的是
| A.Zn → ZnCl2 | B.Cl2 → HClO |
| C.CaCO3 → CO2 | D.CuO → CuSO4 |
下列溶液中Cl-浓度最大的是
| A.200mL 2 mol·L—1 MgCl2溶液 |
| B.1000mL 2.5 mol·L—1 NaCl溶液 |
| C.300mL 5 mol·L—1 KCl溶液 |
| D.250mL 1 mol·L—1 AlCl3溶液 |
设NA表示阿伏加德罗常数,下列叙述中正确的是
| A.常温常压下,11.2L氧气所含的原子数为NA |
| B.1.8g的NH4+离子中含有的电子数为11NA |
| C.常温常压下,48gO3含有的氧原子数为3NA |
| D.5.6g金属铁与足量稀盐酸反应时失去的电子数为0.3NA |
已知aAm+与bBn-具有相同的核外电子排布,则下列关系正确的是
| A.a=b+m+n | B.a=b-m+n | C.a=b+m-n | D.a=b-m-n |