某课外活动小组做了一个有趣的实验:将2 g铝粉和3 g碘粉小心混合均匀,分为质量相等的3份,分别进行如下实验,现将实验记录列表如下:
| 第一组 |
加入0.5 g水 |
很快产生火花 |
| 第二组 |
加入1 g胆矾 |
约需30 s产生火花 |
| 第三组 |
加入1 g无水硫酸铜 |
1 min时仍没有产生火花 |
根据上述实验事实作出的推断错误的是( )
| A.水能增大铝和碘反应的速率 |
| B.第一组实验中铝和碘发生了化合反应生成了AlI3 |
| C.第一组和第二组实验中还能观察到紫色的烟 |
| D.第三组实验中铝和硫酸铜发生了置换反应 |
下面说法正确的是( )
| A.含有羟基的化合物一定属于醇类 |
| B.酚和醇都含有羟基,但其化学性质不完全相同 |
| C.分子中含有苯环和羟基的化合物一定是酚 |
| D.Na2SO3、Na2O2、CaO、苯酚久置于空气中,颜色均有变化 |
某同学欲检验火柴燃烧后的气体中是否含有CO2,他应采用下列方法中的( )
| A.通入澄清的石灰水中 |
| B.先通入足量NaHCO3溶液中,再通入澄清石灰水中 |
| C.通入品红溶液中 |
| D.先通入足量溴水中,再通入澄清石灰水中 |
检验下列有机物的方法中正确的是(双选)( )
| A.向氯仿中加入AgNO3溶液检验其含有氯元素 |
| B.用KMnO4酸性溶液鉴别乙烯和乙炔 |
| C.用FeCl3溶液鉴别苯和苯酚 |
| D.用新制Cu(OH)2悬浊液鉴别乙醇、乙醛和乙酸 |
今有一混合物的水溶液,只可能含有以下离子中的若干种:K+、NH4+、Cl-、Mg2+、Ba2+、CO32-、SO42-,现取三份100 mL溶液进行如下实验:
(1)第一份加入AgNO3溶液有沉淀产生
(2)第二份加足量NaOH溶液加热后,收集到气体0.04 mol
(3)第三份加足量BaCl2溶液后,得干燥沉淀6.27 g,经足量盐酸洗涤、干燥后,沉淀质量为2.33 g。
根据上述实验,以下推测正确的是(双选)( )
| A.K+一定存在 |
| B.100 mL溶液中含0.01 mol CO32- |
| C.Cl-可能存在 |
| D.Ba2+一定不存在,Mg2+可能存在 |
如图装置可用于收集SO2并验证其某些化学性质,下列说法正确的是( )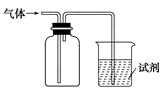
| 选项 |
试剂 |
现象 |
结论 |
| A |
KMnO4酸性溶液 |
溶液褪色 |
SO2有氧化性 |
| B |
品红溶液 |
溶液褪色 |
SO2有漂白性 |
| C |
NaOH溶液 |
无明显现象 |
SO2与NaOH溶液不反应 |
| D |
紫色石蕊试液 |
溶液变红色后不褪色 |
SO2有酸性、没有漂白性 |