在室温条件下,保存下列药品的方法不正确的是( )
| A.氢氧化钠用带玻璃塞的玻璃瓶保存 | B.保存液溴要加少量水形成液封 |
| C.硝酸银溶液装在棕色瓶中避光保存 | D.钠保存在煤油中 |
 在下列给定条件的溶液中,一定能大量共存的离子组是
在下列给定条件的溶液中,一定能大量共存的离子组是
A.无色溶液: 、、H+、 、、H+、 、 、 |
B.能使pH试纸呈红色的溶液:Na+、NH+4、 、 、 |
C.FeCl2溶液:K+、、Na+、、 、、 、、 |
D. ="0.1" mol/L的溶液:Na+、K+、 ="0.1" mol/L的溶液:Na+、K+、 、 、 |
下列叙述正确的是
A.将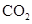 通入 通入 溶液中至饱和,无沉淀产生;再通入 溶液中至饱和,无沉淀产生;再通入 ,产生沉淀 ,产生沉淀 |
B.在稀硫酸中加入铜粉,铜粉不溶解;再加入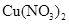 固体,铜粉仍不溶解 固体,铜粉仍不溶解 |
C.向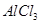 溶液中滴加氨水,产生白色沉淀;再加入过量 溶液中滴加氨水,产生白色沉淀;再加入过量 溶液,沉淀消失 溶液,沉淀消失 |
D.纯锌与稀硫酸反应产生氢气的速率较慢;再加入少量 固体,速率不改变 固体,速率不改变 |
用NA表示阿伏加德罗常数的值。下列叙述正确的是
A.25℃时,PH=13的1.0L Ba(OH)2溶液中含有的 数目为0.2NA 数目为0.2NA |
| B.标准状况下,2.24L Cl2与过量稀NaOH溶液反应,转移的电子总数为0.2NA |
| C.室温下,21.0g乙烯和丁烯的混合气体中含有的碳原子数目为1.5NA |
| D.标准状况下,22.4L 甲醇中含有的氧原子数为1.0NA |
下列有关实验结论正确的是
A.向某溶液中加入盐酸酸化的氯化钡溶液,有白色沉淀生成,该溶液中一定含有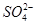 |
| B.向某溶液中加入2滴KSCN溶液,溶液不显红色。再向溶液中加入几滴新制的氯水,溶液变为红色,该溶液中一定含有Fe2+ |
C.将某气体通入品红溶液中,品红溶液褪色,该气体一定是 |
| D.将少量某物质的溶液滴加到新制的银氨溶液中,水浴加热后有银镜生成,该物质一定属于醛类 |
下列说法正确的是
| A.明矾水解形成的Al(OH)3胶体能吸附水中悬浮物,可用于水的净化 |
| B.通电时,溶液中的溶质粒子分别向两极移动,胶体中的分散质粒子向某一极移动 |
| C.溶液中溶质粒子的运动有规律,胶体中分散质粒子的运动无规律,即布朗运动 |
D.电解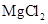 饱和溶液,可制得金属镁 饱和溶液,可制得金属镁 |