溴化碘(IBr)的化学性质与卤素单质相似,能与大多数金属反应生成金属卤化物,和某些非金属反应生成相应的卤化物,跟水反应的化学方程式为IBr+H2O====HBr+HIO。下列有关IBr的叙述中,不正确的是( )
| A.IBr是双原子分子 |
| B.在很多反应中,IBr是氧化剂 |
| C.和NaOH溶液反应生成NaI和NaBrO |
| D.和水反应时,IBr既是氧化剂,又是还原剂 |
硅酸盐与二氧化硅一样,都是以硅氧四面体作为基本结构单元。硅氧四面体可以用投影图表示成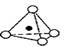 ,其中O表示氧原子,中心黑点表示硅原子。硅氧四面体通过不同方式的连接可以组成各种不同的多聚硅酸根离子。下图为某无限长单链的多聚硅酸根离子:
,其中O表示氧原子,中心黑点表示硅原子。硅氧四面体通过不同方式的连接可以组成各种不同的多聚硅酸根离子。下图为某无限长单链的多聚硅酸根离子:
试确定该阴离子中硅原子与氧原子的个数之比为
| A.1︰2 | B.1︰3 | C.1︰4 | D.2︰5 |
A、B、C、D、E五种物质均含有同一元素,且A为单质,有如图所示的转化关系。则下列判断不正确的是
A.若A、B、C、D、E中同一元素的价态均不相同,则A为气态单质
B.若A为金属钠,则由1molD完全反应生成C时,一定有1mol电子转移
C.若A为非金属硫,则④的反应类型既可以是氧化还原反应又可以是复 分解反应
D.若A为金属铁,则化合物C和D均可以由化合反应生成
下列离子方程式不正确的是
| A.NaHSO4溶液和Ba(OH)2溶液充分反应后溶液呈中性: Ba2+ + 2OH- + 2H+ + SO42- = BaSO4↓ + 2H2O |
| B.次氯酸钙溶液中通入过量的二氧化硫气体: ClO-+H2O+SO2=HSO3-+HClO |
| C.硫酸亚铁溶液中加入用硫酸酸化的过氧化氢溶液: 2Fe2++2H++H2O2=2Fe3++2H2O |
| D.少量CO2加入到苯酚钠溶液中 |
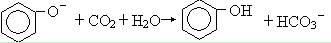
NA表示阿伏加德罗常数的值,下列说法正确的是
| A.标况下,22.4LNO2气体中含有NA个氮原子 |
| B.在Cu-Zn原电池中,正极产生1.12LH2时,负极产生了0.05 NA 个Zn2+ |
| C.常温常压下,1molCl2与足量的Fe反应转移3NA个电子 |
| D.标况下,将m1克锌加入到m2克20%的盐酸中放出nLH2,则转移电子数为nNA/11.2 |
2010年诺贝尔物理学奖授予曼彻斯特大学的两位科学家,以表彰他们在石墨烯材料方面的卓越研究。石墨烯是由石墨剥离而成的单层片状结构的新材料(结构如图),性质稳定、导电性好,有望代替硅引发电子工业革命。下列说法中正确的是 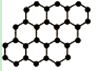
| A.石墨烯之所以稳定主要是因为碳原子间都以共价键相结合 |
| B.石墨烯的发现又为碳的同位素家族增添了一种新的核素 |
| C.由于石墨烯为原子晶体,所以石墨烯应具有很高的熔点 |
| D.石墨烯属于烯烃类的物质,因此在一定条件下可与氢气发生加成反应。 |