(6分) “神舟”7号宇宙飞船是靠长征Ⅱ(F)型运载火箭发射升空的。该火箭所用的燃料是偏二甲肼〔(CH3)2N—NH2〕,氧化剂是N2O4,产物是氮气、二氧化碳和水。
(1)火箭点火瞬间,逸出的红棕色气体是_______,产生该气体的化学反应方程式为
_________。
(2)偏二甲肼在N2O4中燃烧的化学方程式为_________________________,当有1 mol偏二甲肼燃烧时,转移电子的物质的量为___________。
(1)要配制浓度约为2mol/L的NaOH溶液100ml,下面操作正确的是
①称取8g NaOH固体,放入250ml烧杯中,用100ml量筒量取100ml蒸馏水,加入烧杯中,同时不断搅拌至固体溶解
②称取8g NaOH固体,放入100ml量筒中,边搅拌,边慢慢加入蒸馏水,待固体完全溶解后用蒸馏水稀释至100ml
③称取8g NaOH固体,放入100ml容量瓶中,加入适量蒸馏水,振荡容量瓶使固体溶解,再加入水到刻度线,盖好瓶塞,反复摇匀
④用100ml量筒量取40ml 5mol/L NaOH溶液,倒入250ml烧杯中,再用同一量筒取60ml蒸馏水,不断搅拌下,慢慢倒入烧杯中
(2)有下列八种物质 ①NH4Cl ②NaOH ③FeCl3④NaHCO3⑤Al ⑥CH3COOH ⑦盐酸 ⑧H2CO3
(A)属于强电解质的是(填序号)
(B)既与盐酸反应又与氢氧化 钠反应的是(填序号)
钠反应的是(填序号)
(C)将③的饱和溶液滴 入沸水中,继续加热可得红褐色液体,此液体不具有
入沸水中,继续加热可得红褐色液体,此液体不具有 的性质是A.光束通过该液体时形成光亮的“通路”
的性质是A.光束通过该液体时形成光亮的“通路”
B.插入电极通过直流电后,有一极附近液体颜色加深
C.向该液体中加入硝酸银溶液,无沉淀产生
D.将该液体加热蒸干、灼烧后,有氧化物生成
本题包括A、B两小题,分别对应于“物质结构与性质”和“实验化学”两个选修模块的内容。请选定其中一题,并在相应的答题区域内作答。若两题都做,则按A题评分。
A.砷(As)在地壳中含量不大,但砷的化合物却是丰富多彩。
(1)基态砷原子的电子排布式为 ▲;砷与溴的第一电离能较大的是 ▲。
(2)AsH3是无色稍有大蒜味气体。AsH3的沸点高于PH3,其主要原因是 ▲。
(3)Na3AsO4可作杀虫剂。AsO43-的空间构型为 ▲,与其互为等电子体的一种分子为 ▲。
(4)某砷的氧化物俗称“砒霜”,其分子结构如右图所示。该化合物的分子式为 ▲,As原子采取 ▲杂化。
(5)GaAs等是人工合成的新型半导体材料,其晶体结构与金刚石相似。GaAs晶体中,每个As与 ▲个Ga相连,As与Ga之间存在的化学键有 ▲(填字母)。
A.离子键 B.σ键 C.π键  D.氢键 E.配位键 F.金属键 G.极性键
D.氢键 E.配位键 F.金属键 G.极性键
B.某研究小组以苯甲醛为原料,制备苯甲酸和苯甲醇。反应原理如下: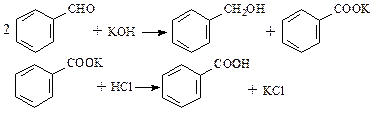
有关物质的部分物理性质如下:
| 熔点/℃ |
沸点/℃ |
溶解性 |
|
| 苯甲醛 |
—26 |
179 |
微溶于水,易溶于乙醇、乙醚 |
| 苯甲酸 |
122 |
249 |
微溶于水,易溶于乙醇、乙醚 |
| 苯甲醇 |
-15.3 |
205.0 |
稍溶于水,易溶于乙醇、乙醚 |
| 乙醚 |
-116.2 |
34.5 |
微溶于水,易溶于乙醇 |
实验步骤:
(1)在250 mL锥形瓶中,放入9 g KOH和9 mL水,配成溶液,冷却至室温。加入10.5 g新蒸馏的苯甲醛,塞紧瓶塞,用力振荡,使之变成糊状物,放置24 h。
①苯甲醛要求新蒸馏的,否则会使 ▲(填物质名称)的产量相对减少。
②用力振荡的目的是 ▲。
(2)分离苯甲醇
①向锥形瓶中加入30 mL水,搅拌,使之完全溶解。冷却后倒入分液漏斗中,用30 mL乙醚萃取苯甲醇(注意留好水层)。30 mL 乙醚分三次萃取的效果比一次 萃取的效果 ▲(填“好”或“差”)。
萃取的效果 ▲(填“好”或“差”)。
②将醚层依次用饱和亚硫酸氢钠溶液、饱和碳酸钠溶液和水各5 mL洗涤,再用无水硫酸镁干燥。将干燥后的乙醚溶液转移到100 mL蒸馏烧瓶中,投入沸石,连接好普通蒸 馏装置,加热蒸馏并回收乙醚,应选择的加热方法是 ▲(填字母代
馏装置,加热蒸馏并回收乙醚,应选择的加热方法是 ▲(填字母代 号)。
号)。
A.水浴加热 B.油浴加热 C.沙浴加热D.用酒精灯直接加热
③改用空气冷凝管蒸馏,收集 ▲℃的馏分。
(3)制备苯甲酸
在乙醚萃取过的水溶液中,边搅拌边加入浓盐酸酸化至pH=3.5左右。 冷却使结晶完全,抽滤,洗涤、干燥。抽滤完毕或中途停止抽滤时,应先 ▲。
冷却使结晶完全,抽滤,洗涤、干燥。抽滤完毕或中途停止抽滤时,应先 ▲。
草酸亚铁可用于合成锂电池的正极材料硅酸亚铁锂(Li2FeSiO4)等,其制备过程主要包括:
a.将硫酸亚铁铵【(NH4)2Fe(SO4)2·6H2O】晶体溶于适量蒸馏水,加入适量稀硫酸酸化。
b.将上述溶液煮沸,逐滴加入H2C2O4溶液,直至沉淀完全。
c.静置、倾去上层清液、过滤、洗涤、50℃以下烘干。试回答下列问题:
(1)配制(NH4)2Fe(SO4)2·6H2O溶液时,需加入少量稀硫酸,目的是 ▲。
(2)将制得的产品(FeC2O4·2H2O)在氩气气氛中进行热重分析,结果如右图(TG%表示残留固体质量占原样品总质量的百分数)。
① 则A-B发生反应的化学方程式为: ▲。
② 精确研究表明,B-C实际是分两步进行的,每步释放一种气体,其中第一步释放的气体相对分子质量较第二步的小,试写出B-C两步反应的方程式:▲、▲;
(3)Li2CO3、FeC2O4·2H2O和SiO2粉末均匀混合,在800℃.
的氩气中烧结6小时,即可制成硅酸亚铁锂。①合成硅酸
亚铁锂的化学方程式为:▲。
②该锂电池放电时的总反应式为LiFeSiO4+Li=Li2FeSiO4,
写出相应的电极反应式:
正极▲、负极▲。
(1 0分)汽车尾气中含有CO、NO2
0分)汽车尾气中含有CO、NO2 等有毒气体,对汽车加装尾气净化装置,可使有毒气体相互反应转化成无毒气体。
等有毒气体,对汽车加装尾气净化装置,可使有毒气体相互反应转化成无毒气体。
(1)汽油在不同空/燃比(空气与燃油气的体积比)时尾气的主要成分不同,空/燃比较小时的有毒气体主要是 ▲(填化学式)。
(2)人们把拆开1 mol化学键所吸收的能量看成该化学键的键能。
已知:N2、O2分子中化学键的键能分别是946 kJ·mol-1、497 kJ·mol-1。
查阅资料获知如下反应的热化学方程式:
N2(g)+O2(g)=2NO(g)ΔH=+180 kJ·mol-1
N2(g)+2O2(g)=2NO2(g)ΔH=+68 kJ·mol-1
2C(s)+O2(g)=2CO(g) ΔH=-221 kJ·mol-1
C(s)+O2(g)=CO2 (g) ΔH=-393.5 kJ·mol-1
(g) ΔH=-393.5 kJ·mol-1
① 一定条件下,N2与O2反应生成NO能够自发进行,其原因是 ▲;NO分子中化学键的键能为 ▲kJ·mol—1。
② CO与NO2反应的热化学方程式为4CO(g)+2NO2(g)=4CO2(g)+N2(g) ΔH= ▲。对于该反应,温度不同(T2>T1)、其他条件相同时,下列图像正确的是 ▲
ΔH= ▲。对于该反应,温度不同(T2>T1)、其他条件相同时,下列图像正确的是 ▲ (填代号)。
(填代号)。
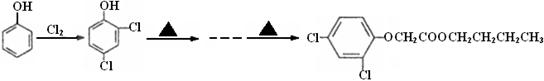
CYP73A1炔抑制剂的合成路线如下: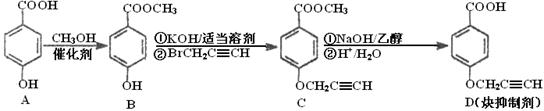
(1)化合物A核磁共振氢谱有______▲______种蜂。
(2)化合物C中含氧官能团有_______▲________、_______▲_______(填名称)。
(3)鉴别化合物B和C最适宜的试剂是____________▲________。
(4)写出A—B的化学方程式_______________▲______________。
(5)B的同分异构体很多,符合下列条件的异构体有_______▲_______种。
①苯的衍生物②含有羧基和羟基 ③分子中无甲基
(6)试以苯酚、氯乙酸钠(ClCH2COONa)、正丁醇为原料(无机试剂任用),结合题中有关信息,请补充完整的合成路线流程图。